向20 mL 0.20 mol/L的NaOH溶液中,缓缓通入一定量的CO2气体,将溶液在一定条件下小心地蒸干,若得到白色固体为纯净物,则通入CO2的体积为________(标准状况).写出反应的离子方程式:___________.
将上述白色固体加水溶解,加盐酸至中性,再蒸干得白色固体,质量为________g.
44.8 mL或89.6 mL CO2+2OH-===CO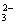 +H2O或OH-+CO2===HCO
+H2O或OH-+CO2===HCO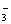 0.23
0.23
本题考查NaOH溶液与CO2反应,由于二者物质的量不同,产物也会不同,同时考查离子方程式的书写,利用元素守恒进行有关计算的能力.
CO2与NaOH发生反应可能的离子方程式为:
ⅰ)CO2+2OH-=CO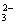 +H2O
+H2O
1 2
n1(CO2) n1(OH-)
ⅱ)CO2+OH-=HCO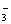
1 1
n2(CO2) n2(OH-)
列出关系式:
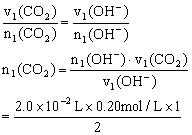
=2.0×10-3 mol
V1(CO2)=n1(CO2)×Vm
=2.0×10-3 mol×22.4 L/mol
=44.8 mL
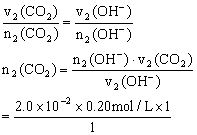
=4.0×10-3 mol
V2(CO2)=n2(CO2)×Vm
=4.0×10-3 mol×22.4 L/mol=89.6 mL
由关系式:
NaOH ~ NaCl
1 1
n(NaOH) n(NaCl)
n(NaCl)=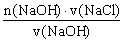

=4.0×10-3 mol
m(NaCl)=n(NaCl)×58.5 g/mol=0.23 g
