问题
实验题
某学生想制作一种家用环保型消毒液发生器,用石墨作电极电解饱和氯化钠溶液,通电便可制得有较强杀菌能力的消毒液,他设计了如图三套装置。
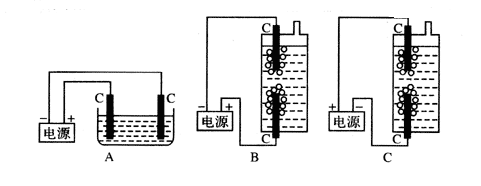
装置A (“能”或“不能”)用于消毒液发生器,简述理由 ;
用化学方程式表示装置B的反应原理: ;上图装置哪一个更好?简述原因 。
答案
不能,装置A显然不能保证氯气和NaOH的充分接触;
2NaCl+2H2O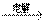 2NaOH+H2↑+Cl2↑ Cl2+2NaOH=NaClO+NaCl+H2O
2NaOH+H2↑+Cl2↑ Cl2+2NaOH=NaClO+NaCl+H2O
装置B,装置B与装置C的区别是把阳极设计在装置的下部或上部,B设计能确保在阳极生成的氯气上升时,与阴极产物NaOH充分接触反应,达到制备的目的。
该制备的反应原理并不复杂,是通过电解饱和食盐水后产生的Cl2与NaOH反应生成NaClO,从而达到制备目的,反应原理:2NaCl+2H2O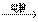 2NaOH+H2↑+Cl2↑(阳极产物)Cl2+2NaOH=NaClO+NaCl+H2O由于电解食盐水时氯气是阳极产物,而NaOH是阴极产物,因此,如何让两极的产物充分接触反应是设计装置的关键。
2NaOH+H2↑+Cl2↑(阳极产物)Cl2+2NaOH=NaClO+NaCl+H2O由于电解食盐水时氯气是阳极产物,而NaOH是阴极产物,因此,如何让两极的产物充分接触反应是设计装置的关键。
