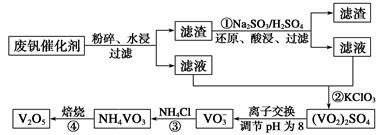
(14分)为回收利用废钒催化剂(含有V2O5、VOSO4及不溶性残渣),科研人员最新研制了一种离子交换法回收钒的新工艺,主要流程如下:
部分含钒物质在水中的溶解性如下:
| 物质 | VOSO4 | V2O5 | NH4VO3 | (VO2)2SO4 |
| 溶解性 | 可溶 | 难溶 | 难溶 | 易溶 |
⑴工业由V2O5冶炼金属钒常用铝热剂法,写出该反应的化学方程式 。
⑵图中所示滤液中含钒的主要成分为 (写化学式)。
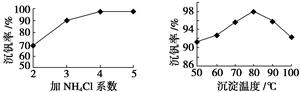
⑶该工艺中反应③的沉淀率(又称沉钒率)是回收钒的关键之一,该步反应的离子方程式 ;沉钒率的高低除受溶液pH影响外,还需要控制氯化铵系数(NH4Cl加入质量与料液中V2O5的质量比)和温度。根据下图判断最佳控制氯化铵系数和温度为 、 。
⑷用硫酸酸化的H2C2O4溶液滴定(VO2)2SO4溶液,以测定反应②后溶液中含钒量,完成反应的离子方程式为□VO2++□H2C2O4+□_____=□VO2++□CO2↑+□H2O。
⑸全矾液流电池的电解质溶液为VOSO4溶液,电池的工作原理为VO2++V2++2H+ 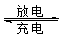 VO2++H2O+V3+,电池充电时阳极的电极反应式为 。
VO2++H2O+V3+,电池充电时阳极的电极反应式为 。
⑴ 3V2O5+10Al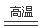 5Al2O3+6V;⑵VOSO4; ⑶ NH4++VO3—=NH4VO3↓; 4;80℃ ;
5Al2O3+6V;⑵VOSO4; ⑶ NH4++VO3—=NH4VO3↓; 4;80℃ ;
⑷ 2VO2++H2C2O4+2H+ = 2VO2++2CO2↑+2H2O ⑸ VO2++H2O-e-=VO2++2H+
题目分析:⑴用V2O5通过铝热反应制取V的方程式为:3V2O5+10Al 5Al2O3+6V。⑵根据流程图及题目提供的物质的溶解性信息可知:在图中所示滤液中含钒的主要成分为VOSO4;⑶向含有VO3—的溶液中加入NH4Cl,发生反应得到NH4VO3沉淀的两种方程式是NH4++VO3—=NH4VO3↓;由于在氯化铵系数是4、反应温度为80℃时沉钒率最高。因此最佳控制氯化铵系数和温度为4;80℃。⑷根据电子守恒、电荷守恒及元素的原子个数守恒可知缺项为H+,相应的两种方程式是2VO2++H2C2O4+2H+ = 2VO2++2CO2↑+2H2O;⑸根据全矾液流电池在充电时的工作原理方程式可知: 电池充电时阳极的电极反应式为VO2++H2O-e-=VO2++2H+。
5Al2O3+6V。⑵根据流程图及题目提供的物质的溶解性信息可知:在图中所示滤液中含钒的主要成分为VOSO4;⑶向含有VO3—的溶液中加入NH4Cl,发生反应得到NH4VO3沉淀的两种方程式是NH4++VO3—=NH4VO3↓;由于在氯化铵系数是4、反应温度为80℃时沉钒率最高。因此最佳控制氯化铵系数和温度为4;80℃。⑷根据电子守恒、电荷守恒及元素的原子个数守恒可知缺项为H+,相应的两种方程式是2VO2++H2C2O4+2H+ = 2VO2++2CO2↑+2H2O;⑸根据全矾液流电池在充电时的工作原理方程式可知: 电池充电时阳极的电极反应式为VO2++H2O-e-=VO2++2H+。
