问题
填空题
在饱和Na2CO3溶液中通入二氧化碳会有晶体析出,在饱和NaCl溶液中通入CO2则不发生化学反应。若在饱和NaCl溶液中通入氨气后,再通入CO2则会有晶体析出,简述其原因并写出相应的化学方程式。
答案
饱和Na2CO3溶液中通入CO2时,所发生的化学反应是:Na2CO3+CO2+H2O====
2NaHCO3;在饱和NaCl溶液中通入足量氨气以后再通入CO2时,则发生以下反应:
NH3+CO2+H2O====NH4HCO3
NH4HCO3+NaCl====NH4Cl+NaHCO3↓
其中NaHCO3溶解度最小,故有NaHCO3的晶体析出。
在Na2CO3饱和溶液中通入CO2时,由于Na2CO3易溶于水,且发生反应Na2CO3+CO2+H2O
====2NaHCO3,而生成的NaHCO3溶解度小,所以随着CO2气体的通入,会有NaHCO3晶体析出。
氯化钠是强酸盐,CO2是弱酸的酸酐,根据复分解反应规律,CO2不能与NaCl溶液反应。通入足量氨气的饱和NaCl溶液中再通入CO2时,CO2跟氨水反应生成NH4HCO3,当溶液中Na+、Cl-、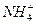 、
、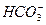 等离子浓度都较大时,首先是微溶于水的NaHCO3析出。
等离子浓度都较大时,首先是微溶于水的NaHCO3析出。
