在体积固定的密闭容器中,进行如下化学反应:N2O4(g) 2NO2(g),其化学平衡常数K和温度t的关系如下表:
2NO2(g),其化学平衡常数K和温度t的关系如下表:
| t /℃ | 80 | 100 | 120 |
| K | 1.80 | 2.76 | 3.45 |
请回答下列问题:
(1)该反应的化学平衡常数表达式K= 。
(2)该反应为 反应(填“吸热”或“放热”)。
(3)判断该反应达到化学平衡状态的依据是 。
A.容器内混合气体密度不变
B.混合气体中c(NO2)不变
C.0.5mol N2O4分解的同时有1 mol NO2生成
(4)在80℃时,将2.80molN2O4气体充入2L固定容积的密闭容器中,一段时间后对该容器内的物质进行分析,得到如下数据:
  | 0 | 20 | 40 | 60 | 80 | 100 |
| n(N2O4) | 2.80 | A | 2.00 | c | d | 1.60 |
| n(NO2) | 0 | 0.96 | b | 2.08 | 2.40 | 2.40 |
①b的值为 ;
②N2O4的平衡转化率为 ;
③20s~40s内用N2O4表示的平均反应速率υ(N2O4)= 。
(1)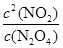 (1分) (2) 吸热(2分) (3) B (2分)
(1分) (2) 吸热(2分) (3) B (2分)
(4)①1.60 (2分) ②42.9% 或0.429(2分) ③0.008 mol·L-1·S-1(2分)
题目分析:(1)化学平衡常数是在一定条件下,当可逆反应达到平衡状态时,生成物浓度的幂之积和反应物浓度的幂之积的比值,所以根据反应的化学方程式可知,该反应的平衡常数表达式K=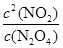 。
。
(2)根据表中数据可知,随着温度的升高,平衡常数逐渐增大。这说明升高温度平衡向正反应方向移动,因此正方应是吸热反应。
(3)在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态,据此可以判断。A、密度是混合气的质量和容器容积的比值,在反应过程中质量和容积始终是不变的,因此密度始终是不变,所以容器内混合气体密度不变不能说明反应达到平衡状态,A不正确;B、混合气体中c(NO2)不变可以说明反应得到平衡状态,B正确;C、根据反应式可知,0.5mol N2O4分解的同时一定有1 mol NO2生成,所以不能说明反应达到平衡状态,C不正确,答案选B。
(4)①根据表中数据可知,反应进行到20s时NO2的物质的量是0.96mol所以消耗N2O4的物质的量是0.96mol÷2=0.48mol,则剩余N2O4的物质的量=2.80mol-0.48mol=2.32mol,即A=2.32mol。从20s进行到40s消耗N2O4的物质的量=2.32mol-2.00mol=0.32mol,所以生成NO2的物质的量=0.32mol×2=0.64mol,则b=0.96mol+0.64mol=1.60mol,即b=1.60mol。
②根据表中数据可知,反应进行到80s时NO2的物质的量不再发生变化,说明反应达到平衡状态,此时消耗N2O4的物质的量=2.40mol÷2=1.20mol,所以N2O4的转化率=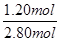 ×100%=42.9%。
×100%=42.9%。
③20s~40s内消耗N2O4的浓度=0.32mol÷2L=0.16mol/L,所以用N2O4表示的平均反应速率υ(N2O4)=0.16mol/L÷20s=0.008 mol·L-1·S-1。
