碘及其化合物在人类活动中占有重要地位。
(1)加碘食盐中含有碘酸钾(KIO3),工业上以电解法制备碘酸钾,电解设备如图所示。先将一定量的碘溶于过量氢氧化钾溶液,发生反应:
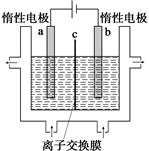
3I2+6KOH=5KI+KIO3+3H2O,再将该溶液加入 (阴极、阳极)区,另将氢氧化钾溶液加入另外一个区。使用 (阴、阳)离子交换膜,在阳极发生的电极反应式: 。
(2)碘化氢不稳定,分解反应的热化学方程式是2HI(g)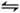 I2(g)+H2(g) ΔH="+9.48" kJ·mol-1已知ΔS>0
I2(g)+H2(g) ΔH="+9.48" kJ·mol-1已知ΔS>0
①该反应属于( )
A.任何温度均自发 B.任何温度均不自发 C.高温自发 D.低温自发
②一定条件下,反应在一个带有活塞的密闭容器中达到平衡,下列说法中不正确的是( )
A.恒温,缩小体积,平衡常数不变
B.恒温,缩小体积,平衡不移动,颜色加深
C.恒容,升温,正向反应速率和逆向反应速率均增大
D.恒容,在容器中若投入2mol HI,达到平衡时吸收9.48 kJ 的热量
③一定温度下,平衡常数K=1/4,在2L的容器中,加入4molHI发生反应达到平衡,HI的转化率 。
(1)阳极 阴 I-+6OH-—6e-=IO3-+3H2O (2)①C②D ③0.5
题目分析:(1)由题意知电解法制备碘酸钾的原理为在KOH存在的条件电解KI和KIO3的混合液,反应的实质是碘离子发生失电子的氧化反应,最终生成碘酸根离子,结合电解原理电解池的阳极发生失电子的氧化反应,所以KI和KIO3的混合液应加在与电源正极相连的阳极区,即装置中的a极区;根据电极方程式书写原则原子守恒和电荷守恒,电极反应式为:I-+6OH-—6e-=IO3-+3H2O,该极区反应消耗OH—,应有加在阴极区的KOH溶液补充,离子交换膜应允许阴离子通过,为阴离子交换膜。
(2)①该反应ΔH>0,ΔS>0,根据反应方向的判据可知高温时ΔH—TΔS<0,能自发进行;选C.
②A、平衡常数的影响因素为温度,正确;B、该反应两边气体物质系数相等,恒温,缩小体积,平衡不移动,但各物质的浓度增大,颜色加深,正确;C、升温反应速率加快,正确;D、可逆反应的特点是不能进行到底,投入2mol HI,达到平衡时吸收的热量小于9.48 kJ,错误。
③ 设转化的碘化氢为x,利用三段法得出各物质的平衡浓度,代入平衡常数表达式求出碘化氢的平衡浓度,代入转化率计算公式计算可得。
