(1)写出电解饱和食盐水的离子方程式
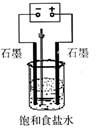
(2)用右图所示装置电解500mL2mol·L-1食盐水可制取一种消毒液,在通电过程中不断搅拌溶液(使阳极产物全部溶解在溶液中)溶液的pH(填写字母)
A.逐渐增大;
B.逐渐减小;
C.保持不变
当阳极有氧气生成时,停止通电最终所得溶液中的溶质主要成分是 ;
假设电解过程中阳极产物无逸出,溶液加水至500mL,消毒液的浓度是 mol·L-1
(3)向上述制取的消毒液中通入CO2气体,可以增强消毒效果,写出反应的离子方程式
(1)2Cl-+2H2O Cl2↑+H2↑+2OH-(2分)
Cl2↑+H2↑+2OH-(2分)
(2)A;NaClO;(每空1分,共2分) 2(2分)
(3)2ClO-+CO2+H2O 2HClO+CO32-
本题考查电解原理及规律,试题;(1)电解饱和食盐水的离子反应方程式为:2Cl-+2H2O Cl2↑+H2↑+2OH-;(2)电解食盐水,在通电过程中氢氧化钠的浓度逐渐增大,所以溶液的pH将不断增大;阳极产物为氯气与氢氧化钠反应生成NaClO、NaCl、水,当阳极有氧气生成时,说明氯化钠全部电解,最终所得溶液中的溶质主要成分为NaClO;
Cl2↑+H2↑+2OH-;(2)电解食盐水,在通电过程中氢氧化钠的浓度逐渐增大,所以溶液的pH将不断增大;阳极产物为氯气与氢氧化钠反应生成NaClO、NaCl、水,当阳极有氧气生成时,说明氯化钠全部电解,最终所得溶液中的溶质主要成分为NaClO;
根据:2NaCl+2H2O Cl2↑+H2↑+2NaOH Cl2+NaOH=NaCl+NaClO+H2O
Cl2↑+H2↑+2NaOH Cl2+NaOH=NaCl+NaClO+H2O
2NaCl ~ NaClO
1mol 1mol
0.5L×2mol·L-1 n(NaClO)
n(NaClO)=1mol
c(NaClO)=2mol·L-1
(3)消毒液中通入CO2气体,可生成次氯酸,增强消毒效果,
2ClO-+CO2+H2O 2HClO+CO32-
