在体积为10L的容器中,通人一定量的CO和H2O,在850℃时发生如下反应:
CO(g)十H2O(g) 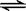 CO2(g)十H2 (g) △H<0 , CO和H2O浓度变化如下图,
CO2(g)十H2 (g) △H<0 , CO和H2O浓度变化如下图,
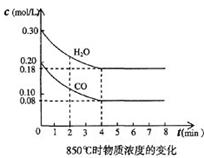
(1) 3min—4min之间反应处于____状态(填平衡、不平衡);
(2)要使反应在8min后,平衡向逆方向移动,可采取的措施是__ ___,要使反应在8min后,反应速率降低,平衡向正方向移动,可采取的措施是________。(填a,b,c,d)
a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度
(3)求出850℃ 时,该反应的平衡常数和CO的平衡转化率(写出详细计算过程)
(1) 不平衡 (2) d , b (各2分)
(3)0.6 (2分)
题目分析:
(1)由图可知3min—4min之间物质的浓度在变化。所以不平衡
(2)a.增加水蒸气,衡向正方向移动 b.降低温度,平衡向逆方向移动 c.使用催化剂,不改变平衡。 d.增加氢气浓度,反应速率降低,平衡向正方向移动。
(3) CO(g) 十 H2O(g)  CO2(g) 十 H2 (g)
CO2(g) 十 H2 (g)
初始浓度(mol/L) 0.2 0.3 0 0
变化浓度(mol/L) 0.12 0.12 0.12 0.12
平衡浓度(mol/L) 0.08 0.18 0.12 0.12
K = c(CO2) c(H2) / c(CO) c(H2O) =" (" 0.12 mol/L *0.12 mol/L ) / (0.08 mol/L* 0.18 mol/L) = 1
CO的平衡转化率 =" 0.12" mol/L / 0.2 mol/L = 0.6
