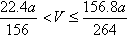将15.6g Na2O2与2.7g Al粉混合后,投入足量的水中,充分反应(设能产生的气体全部放出)。
(1)Na2O2与水反应的化学方程式为 ,15.6g Na2O2在该反应中转移电子的物质的量为 mol。
(2)反应结束时生成的气体在标准状况下为 L。
(3)取a g Na2O2与Al粉组成的混合物,放入适量的水中,固体完全溶解,在标准状况下
放出气体V L,则V的取值范围是 (用含a的代数式表示,结果可不化简)。
(1)(2分)2Na2O2+2H2O=4NaOH+O2↑;(2分)0.2mol (2)(2分)5.6L
(3)(4分)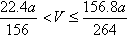
15.6g Na2O2的物质的量为0.2mol;2.7g Al的物质的量为0.1mol;
(1)Na2O2与水反应的化学方程式为:2Na2O2+2H2O=4NaOH+O2↑;1mol Na2O2与水反应转移的电子数为1mol;所以,15.6g Na2O2在该反应中转移电子的物质的量为0.2mol;
(2)15.6g Na2O2与水反应生成0.4mol氢氧化钠,生成0.1mol氧气;生成的氢氧化钠与AL反应的方程式为: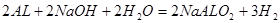 ,所以2.7g Al粉反应后生成氢气0.15mol;所以反应结束时生成的气体在标准状况下为5.6L;
,所以2.7g Al粉反应后生成氢气0.15mol;所以反应结束时生成的气体在标准状况下为5.6L;
(3)