问题
选择题
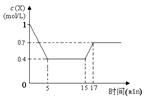
一定条件下,向密闭容器中加入X物质发生反应:3X(g)  Y(g) + Z(g) △H<0,反应一段时间后改变某一个外界条件,反应中各时刻X物质的浓度如下表所示。下列说法中不正确的是
Y(g) + Z(g) △H<0,反应一段时间后改变某一个外界条件,反应中各时刻X物质的浓度如下表所示。下列说法中不正确的是
| 反应时间(min) | 0 | 5 | 15 | 17 | 20 |
| X的浓度(mol·L-1) | 1.0 | 0.4 | 0.4 | 0.7 | 0.7 |
B.5 min时反应达到平衡,该温度下的平衡常数值为0.625
C.15 min时改变的条件可能是降低温度
D.从初始到18 min时,X的转化率为30 %
答案
答案:C
题目分析:由图可知,0~5 min内X的浓度变化量为1mol/L-0.4mol/L=0.6mol/L,故v(X)=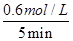 =0.12 mol/(L•min),故A正确;由图可知,0~5 min内X的浓度变化量为1mol/L-0.4mol/L=0.6mol/L,则:
=0.12 mol/(L•min),故A正确;由图可知,0~5 min内X的浓度变化量为1mol/L-0.4mol/L=0.6mol/L,则:
3X(g) Y(g)+Z(g)
Y(g)+Z(g)
开始(mol/L):1 0 0
变化(mol/L):0.6 0.2 0.2
平衡(mol/L):0.4 0.2 0.2
该温度下平衡常数k=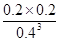 =0.625,故B正确;
=0.625,故B正确;
由图可知,15min时瞬间X的浓度不变,不可能为改变压强,改变条件X的浓度增大,该反应正反应是放热反应,可能为升高温度或增大生成物的物质的量,故C错误;由图可知,从开始到17 min时,X的浓度变化量为1mol/L-0.7mol/L=0.3mol/L,故X的转化率为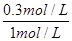 ×100%=30%,故D正确;故选C.
×100%=30%,故D正确;故选C.

