(10分)胃酸过多是常见的胃病。下面是甲、乙两种常见胃药的说明摘要。
甲:(1)白色结晶状粉末;(2)能溶于水,水溶液呈弱碱性;(3)受热分解;(4)遇酸及酸性药物则产生二氧化碳;(5)胃酸过多患者服用后多见胃胀气,甚至有引起溃疡穿孔的危险。
乙:(1)与胃酸的中和作用缓慢持久,可维持3~4小时;(2)凝胶本身覆盖于溃疡面上,具有保护作用,并能吸附H+;(3)可溶于稀酸或氢氧化钠溶液。
(1)请你推测,甲中含有的主要化学成分是 (填化学式,下同);乙中含有的主要化学成分是 。
(2)写出甲中含有的主要化学成分引起胃胀气的离子方程式______________________。
(3)写出乙中含有的主要化学成分分别与稀盐酸和氢氧化钠溶液反应的离子方程式__________________________________、_________________________________。
(10分)(1)NaHCO3 (2分) Al(OH)3 (2分)
(2)HCO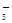 +H+=CO2↑+H2O (2分)
+H+=CO2↑+H2O (2分)
(3)Al(OH)3+3H+=Al3++3H2O (2分) Al(OH)3+OH-=AlO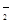 +2H2O(2分)
+2H2O(2分)
题目分析:(1)甲遇酸及酸性药物则产生二氧化碳,说明是碳酸盐或碳酸氢盐。又因为受热易分解,所以甲是碳酸氢钠。乙可溶于稀酸或氢氧化钠溶液,且能吸附H+,所以乙是氢氧化铝。
(2)胃酸中含有氢离子,所以和碳酸氢钠反应的方程式是HCO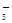 +H+=CO2↑+H2O。
+H+=CO2↑+H2O。
(3)氢氧化铝是两性氢氧化物,既能和酸反应,也能溶于强碱溶液中,反应的离子方程式分别是Al(OH)3+3H+=Al3++3H2O、Al(OH)3+OH-=AlO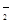 +2H2O。
+2H2O。
点评:关于物质的性质和用途除了需要熟练记住外,还需要灵活运用。
