(13分)钠、氯及其化合物有如下转化关系,请按要求填空:
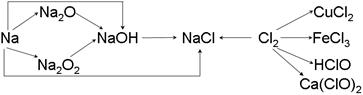
(1)金属钠的密度比水 ,实验室中金属钠通常保存在 中。一小块金属钠投入水中的反应方程式是 。
(2)Na2O2 是 色的固体,Na2O2 的重要用途是 ,有关反应的化学方程式为 。
(3)通常情况下,为了防止污染环境,在做完实验后,多余的氯气应用NaOH溶液吸收,其化学方程式为 。
(4)漂白粉的有效成份是 (填化学式),漂白粉溶于水后,受空气中的CO2作用,产生有漂白、杀菌作用的次氯酸,化学方程式为 。
(13分)(1)小 煤油(各1分) 2Na+ 2H2O=2NaOH+H2↑ (2分)
(2)淡黄 做呼吸面具 (各1分) 2Na2O2+2CO2=2Na2CO3+O2(2分)
(3)Cl2 +2NaOH="NaCl" + NaClO + H2O(2分)
(4)Ca(ClO)2 (1分) Ca(ClO)2 + CO2 + H2O ="=" CaCO3↓+ 2 HClO (2分)
考查钠、氯气及其化合物的性质和有关用途。
(1)金属钠的密度小于水的,由于金属钠极易被氧化和吸水,所以应该不存在煤油中。钠和水反应生成氢氧化和氢气,反应的方程式是2Na+ 2H2O=2NaOH+H2↑ 。
(2)过氧化钠是淡黄色固体,其主要的用途是做呼吸面具的供养剂,反应的方程式是2Na2O2+2CO2=2Na2CO3+O2、2Na2O2+2H2O=4NaOH+O2。
(3)氯气有毒,需要尾气处理,反应的方程式是Cl2 +2NaOH="NaCl" + NaClO + H2O。
(4)漂白粉是混合物,主要成分是次氯酸钙和氯化钙,其有效成份是次氯酸钙;碳酸的酸性强于次氯酸的,所以次氯酸钙能吸收CO2和水蒸气生成次氯酸,反应的方程式是Ca(ClO)2 + CO2 + H2O ="=" CaCO3↓+ 2 HClO。
