问题
填空题
(5分)10℃时加热NaHCO3的饱和溶液,测得该溶液的pH发生如下变化:
| 温度(℃) | 10 | 20 | 30 | 加热煮沸后冷却到50℃ |
| pH | 8.3 | 8.4 | 8.5 | 8.8 |
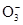 的水解程度增大,故碱性增强。
的水解程度增大,故碱性增强。(1)乙同学认为溶液pH升高的原因是NaHCO3受热分解,生成了Na2CO3,并推断Na2CO3的水解程度大于NaHCO3,该分解反应的化学方程式__________________________________。
(2)丙同学认为甲、乙的判断都不充分。丙认为:只要在加热煮沸的溶液中加入足量的BaCl2溶液,若产生沉淀,则乙判断正确。请写出该过程的离子方程式_____________;上述丙同学的实验__________(填“能”或“不能”)用Ba(OH)2溶液代替BaCl2溶液。
答案
(5分)(1)2NaHCO3 Na2CO3+CO2↑+H2O (2分)
Na2CO3+CO2↑+H2O (2分)
(2)Ba2++C ===BaCO3↓,(2分) 不能 (1分)
===BaCO3↓,(2分) 不能 (1分)
(1)碳酸氢钠不稳定,受热易分解,反应的方程式是2NaHCO3 Na2CO3+CO2↑+H2O。
Na2CO3+CO2↑+H2O。
(2)可溶性的碳酸盐再溶液中能和氯化钡反应生成碳酸钡白色沉淀,反应的方程式是Ba2++C ===BaCO3↓。由于氢氧化钡也能和碳酸氢钠反应生成碳酸钡白色沉淀,所以不能用氢氧化钡溶液代替氯化钡溶液。
===BaCO3↓。由于氢氧化钡也能和碳酸氢钠反应生成碳酸钡白色沉淀,所以不能用氢氧化钡溶液代替氯化钡溶液。
