过氧化钠(Na2O2)是中学常见物质。已知:过氧化钠与CO2反应有气体生成,而将SO2通入过氧化钠粉末中也有气体生成。有人提出CO2、SO2与过氧化钠的反应原理相同,但也有人提出SO2具有较强的还原性,能被过氧化钠氧化生成硫酸钠,CO2无强还原性,反应原理不相同。据此设计如下实验操作进行判断。
实验一:向一定量的过氧化钠固体中通入足量的SO2,取反应后的固体进行实验探究,以证明过氧化物与SO2反应的特点。
(1)提出假设:假设1:反应后固体中只有________,证明SO2未被氧化;
假设2:反应后固体中只有________,证明SO2完全被氧化;
假设3:__________________________证明______________________。
实验探究:实验二:通过测量气体的体积判断发生的化学反应,实验装置如下:

(2)试剂A可以选用________,试剂B的作用是________。
(3)实验测得装置C中过氧化钠质量增加了m1 g,装置D质量增加了m2 g,装置E中收集到的气体为V L(已换算成标准状况下),用上述有关测量数据判断, SO2未被氧化时、完全被氧化的V-m1关系式。
未被氧化:____________,完全被氧化:____________。
(4)若SO2完全被氧化,写出反应的化学方程式: __________________________。
(1)Na2SO3(1分) Na2SO4(1分) Na2SO3和Na2SO4的混合物(1分) SO2被部分氧化(1分)
(2)浓H2SO4 (2分) 吸收未反应的SO2(2分)
(3)V=7m1/30 (2分) V=0 (2分)
(4)SO2+Na2O2= Na2SO4 (2分)
题目分析:根据题目问题:(1)假设1:反应后固体只有 Na2SO3,证明SO2未被氧化;假设2:反应后固体中只有 Na2SO4,证明SO2完全被氧化;假设3:固体为Na2SO3和Na2SO4的混合物;证明SO2部分被氧化;实验二:(2)过氧化钠和水反应,装置A中试剂能吸收水蒸气,所以试剂为浓硫酸,干燥气体除去水蒸气;装置B为测定生成氧气的体积,需要把剩余的二氧化硫除去,因此试剂B装置作用是吸收未反应的SO2。(3)实验测得装置C中过氧化钠质量增加了m1 g,装置D质量增加了m2 g,装置E中收集到的气体为V L(已换算成标准状况下)。若SO2未被氧化、则发生反应:2Na2O2+2SO2=2Na2SO3+O2。依据化学方程式和反应增重计算E中收集的氧气,即
2Na2O2+2SO2=2Na2SO3+O2 反应增重
1mol 96g
 m1g
m1g
解得V=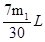 ;若二氧化硫全部被氧化发生的反应为:Na2O2+SO2=Na2SO4;反应过程中无氧气生成,V=0,若0<V<
;若二氧化硫全部被氧化发生的反应为:Na2O2+SO2=Na2SO4;反应过程中无氧气生成,V=0,若0<V<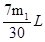 ,则二氧化硫部分被氧化。(4)二氧化硫完全被氧化生成硫酸钠,反应的化学方程式为:SO2+Na2O2═Na2SO4。2和过氧化钠反应的实验探究
,则二氧化硫部分被氧化。(4)二氧化硫完全被氧化生成硫酸钠,反应的化学方程式为:SO2+Na2O2═Na2SO4。2和过氧化钠反应的实验探究
