问题
计算题
某探究小组进行了以下实验:称取9.5g碳酸钠和碳酸氢钠混合物的粉末,向其中加入足量的稀硫酸,将生成的气体通入到足量的澄清石灰水中,充分反应后,过滤、洗涤、干燥,称量所得沉淀的质量为10.0g(假设过程中没有物质损耗)。求该混合物中碳酸钠的质量分数(写出计算过程,结果用分数表示)。
答案
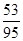
题目分析:设原混合物中碳酸钠和碳酸氢钠的物质的量分别是x与y,则根据总质量可知
106g/mol×x+84g/mol×y=9.5g ①
碳酸钠与碳酸氢钠和稀硫酸反应生成CO2气体,CO2与澄清的石灰水反应生成白色沉淀碳酸钙,即10.0g白色沉淀是碳酸钙,物质的量=10.0g÷100g/mol=0.1mol,则根据碳原子守恒可知生成的CO2的物质的量是0.1mol
根据反应的方程式可知
Na2CO3+H2SO4=Na2SO4+H2O+CO2↑
1mol 1mol
x x
2NaHCO3+H2SO4=Na2SO4+2H2O+2CO2↑
2mol 2mol
y y
因此x+y=0.1mol ②
由①②联立解得x=y=0.05mol
所以原混合物中碳酸钠的质量分数=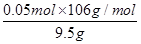 =
=