1862年,比利时化学家索尔维发明了氨碱法制碱,1926年,我国化学家侯德榜创立了
更为进侯德榜制碱法,也叫联合制碱法,两种制碱的生产流程可简要表示如下图:
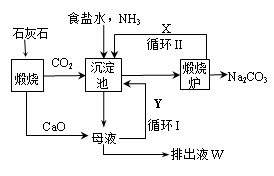
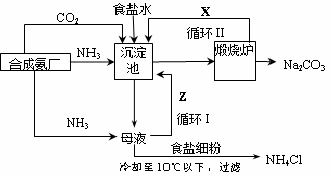
氨碱法生产流程 联合制碱法生产流程
(1)向沉淀池中通入CO2和氨气时,应先通入氨气的原因是 。
(2)沉淀池中发生反应的化学反应方程式是 从沉淀池中分离沉淀的操作是 。
(3)氨碱法生产流程示意图中的Y是 ,从原料到产品,氨碱法总反应过程用化学方程式表示,可写为 。
(4)联合制碱法中从滤液中提取氯化铵晶体的过程推测,所得结论正确是 (选填编号)。
a.常温时氯化铵的溶解度比氯化钠小
b.通入氨气能增大NH4+的浓度,使氯化铵更多析出
c.加入食盐细粉能提高Na+的浓度, 使NaHCO3结晶析出
d.通入氨气能使NaHCO3转化为Na2CO3,提高析出的NH4Cl纯度
(5)联合制碱法相比于氨碱法,氯化钠利用率从70%提高到90%以上,主要是设计了循环Ⅰ,联合制碱法的另一项优点是 。
(6)产品纯碱中含有碳酸氢钠,可以用加热分解的方法测定产品中纯碱的质量分数,已知样品质量为ag,加热至质量不再改变时称重为bg,则纯碱的质量分数为 。
(1)因为CO2溶解度小,而NH3易溶于水,先通入NH3有利于后面CO2的吸收(2分)
(2)NH3+CO2+NaCl+H2O═NaHCO3↓+NH4Cl( 2分,无”↓”扣1分) 过滤(1分)
(3)NH3 ( 2分) CaCO3+2NaCl═Na2CO3+CaCl2( 2分)
(4)bd( 2分)
(5)避免产生大量的含有CaCl2的溶液,或节省石灰窑、蒸氨塔等设备。( 2分)
(6)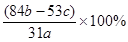 ( 2分)
( 2分)
题目分析:(1)氨气溶解度大,通入氨气后使溶液显碱性,吸收二氧化碳的量增加;(2)沉淀池中氨气、二氧化碳和氯化钠反应生成碳酸氢钠晶体,过滤得碳酸氢钠;(3)沉淀池中的母液是氯化铵溶液,加入的氧化钙和水反应生成氢氧化钙,氢氧化钙和氯化铵反应生成氨气,将氨气在通入沉淀池中循环利用,故Y为氨气;从理论上分析,氨碱法生产过程中,母液中加入氧化钙,和水反应生成的氢氧化钙会和铵盐生成氨气,反应过程中氨气转化为铵盐,铵盐转化为氨气,氨气循环使用,不需要补充氨气;
NaCl+NH3+CO2+H2O═NaHCO3↓+NH4Cl;CaCO3═CaO+CO2↑;CaO+H2O═Ca(OH)2;Ca(OH)2+2NH4Cl═CaCl2+2NH3↑+2H2O;2NaHCO3═Na2CO3+H2O+CO2↑合并得到总化学方程式为:CaCO3+2NaCl═Na2CO3+CaCl2,故答案为: CaCO3+2NaCl═Na2CO3+CaCl2;(4)联碱法中从母液中提取氯化铵晶体的过程中;a、常温时氯化铵的溶解度比氯化钠大,故a错误;b、通氨气作用有增大NH4+的浓度,使NH4Cl更多地析出和使NaHCO3转化为Na2CO3,提高析出的NH4Cl纯度,故b、d正确;c、加入食盐细粉目的是提高Cl-的浓度,促进氯化铵结晶析出,故c错误;(5)联合制碱法与氨碱法比较,其最大的优点是使食盐的利用率提高到96%以上,应用同量的食盐比氨碱法生产更多的纯碱.另外它综合利用了氨厂的二氧化碳和碱厂的氯离子,同时,生产出两种可贵的产品--纯碱和氯化铵.将氨厂的废气二氧化碳,转变为碱厂的主要原料来制取纯碱,这样就节省了碱厂里用于制取二氧化碳的庞大的石灰窑;将碱厂的无用的成分氯离子(Cl-)来代替价格较高的硫酸固定氨厂里的氨,制取氮肥氯化铵.从而不再生成没有多大用处,又难于处理的氯化钙,减少了对环境的污染,并且大大降低了纯碱和氮肥的成本,充分体现了大规模联合生产的优越性,(6)写出碳酸氢钠分解的化学方程式,设固体中含碳酸氢钠的质量为x,当反应掉2mol即168g碳酸氢钠时,固体质量减少62g,根据质量差法计算出固体中含碳酸氢钠的质量,用总质量减去碳酸氢钠的质量得固体中碳酸钠的质量,从而求出质量分数。
