实验目的:探究过氧化钠与水反应后的溶液滴加酚酞试液先变红后退色的原因。
[分析与猜想]
(1)根据过氧化钠与水反应的原理:2Na2O2 + 2H2O =" 4NaOH" + O2↑,往过氧化钠固体完全溶解反应后的溶液中滴加酚酞本应只会变红而不会退色,而实验中发现酚酞变红后又退色。由此提出如下的猜想:
A.氧气有漂白性
B.氢氧化钠有漂白性
C.
[实验与判断] 请完成下列表格:
| 实验编号 | 1 | 2 | 3 |
| 实验装置 | 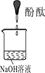 | 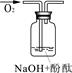 | 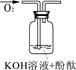 |
| 验证猜想 | C | ||
| 实验现象 | 溶液变红后不退色 | ||
| 实验说明 | 1、2的实验中NaOH溶液是用 (填“氢氧化钠固体”、“氧化钠固体”、“过氧化钠固体”)溶于水配制的。 | ||
(2)根据以上实验分析发现:过氧化钠与水反应过程中,钠元素形成了稳定的化合物,溶液中还生成了一种不很稳定、具有漂白性的物质X,X的化学式是 。
(3)可用右图装置对溶液中不很稳定的物质进行探究,在①处装入的物质是 (填选项,下同),②处装入的物质是 。
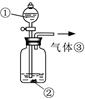
A.酚酞试剂 B.过氧化钠与水反应后的溶液
C.二氧化锰 D.氢氧化钠固体配制的溶液
(4)气体③是 ,过氧化钠与水反应的化学方程式没有写出X来,原因是 。
(1)氧气和氢氧化钠共同作用具有漂白性 B A 氢氧化钠固体(各1分共3分)
(2)H2O2
(3)B C (各1分)
(4)O2(1分) H2O2不稳定,已分解
题目分析:(1)结合A、B,C的猜想是氧气和氢氧化钠共同作用具有漂白性,所以实验1对应的是B,实验3对应的是A;氢氧化钠溶液是用氢氧化钠固体配制的,因为氧化钠固体空气中易变质,造成所配溶液 不纯,过氧化钠固体与水作用除生成氢氧化钠外还会有氧气生成,给实验带来干扰
(2)钠元素形成了稳定的化合物即氢氧化钠,另一种不很稳定、具有漂白性的物质X应是过氧化氢, 其化学式为H2O2
(3)过氧化氢在二氧化锰作催化剂的条件下分解产生氧气,氧气 可用带火星的木条检验,所以①处装
入的物质过氧化钠与水反应后的溶液,选B,②处装入的物质是二氧化锰,选C。
(4)气体③是氧气,因为过氧化氢不稳定,分解产生氧气,所以在书写过氧化钠与水的反应方程式时不写出
