请根据教材上的实验“钠与氯气反应”,完成下列问题。

(1)取一块绿豆大的金属钠(切去氧化层),用滤纸吸净其表面的煤油,放在石棉网上,用酒精灯微热。待钠熔成球状时,将盛有氯气的集气瓶迅速倒扣在钠的上方。根据所学的知识分析该实验存在哪些缺点?
①____________________________________________________;
②____________________________________________________;
③________________。(至少填2条)
(2)某同学根据以上存在的缺点改进实验装置,如图所示:
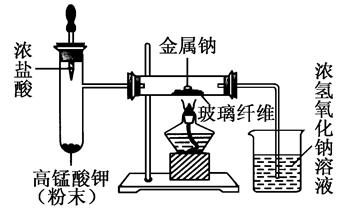
实验步骤:
a.取绿豆粒大的钠,用滤纸吸干表面的煤油,切去氧化层,放入玻璃管中,按图示安装好仪器;
b.慢慢滴加浓盐酸,立即剧烈反应产生氯气;
c.当玻璃管中充满黄绿色气体时,再加热钠,钠熔化并燃烧。
①观察到的实验现象有:当滴加浓盐酸后试管中产生________色气体;钠剧烈燃烧,火焰呈________色且有________生成,反应结束后,管壁上观察到有________生成。
②改进后的实验优点:a.________,b.________,c.______(至少回答2条)。
③写出Na在Cl2中燃烧的化学方程式________________,并用电子式表示产物形成过程________________。
(1)①Na预先在空气中加热,会生成氧化物,可能影响Na在Cl2中燃烧
②预先收集的Cl2在进行实验时可能不够或过量
③实验过程中会造成污染
(2)①黄绿 黄 白烟 白色固体
②a.整个实验过程中氯气保持一定浓度和纯度,避免发生副反应 b.安全可靠,污染少 c.可以避免钠在加热时生成Na2O2
③2Na+Cl2 2NaCl
2NaCl 
上述两个实验的不同在于一静一动。可从操作便利、易控制反应快慢、环境污染等方面分析。
