我国化工专家侯德榜,改进氨碱法设计了“联合制碱法”,为世界制碱工业作出了突出贡献。生产流程如下:
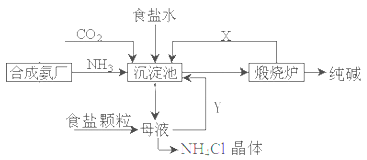
(1)完成有关反应的化学方程式
①沉淀池: NH3+CO2+H2O+NaCl=NaHCO3↓+NH4Cl
②煅烧炉:
(2)联合制碱法的优点表述中,不正确的是___________
A.生产原料为:食盐、NH3、CO2
B.副产物氯化铵可做氮肥
C.生产过程中可循环利用的物质只有CO2
D.原料利用率高
某实验小组,利用下列装置模拟“联合制碱法”的第一步反应。

(3)上述装置中接口连接顺序为 ;
A.a接c;b接f、e接d B.a接d;b接f、e接c
C.b接d;a接e、f接c D.b接c;a接f、e接d
(4)D中应选用的液体为 。
为测定产品纯碱的成分和含量,做如下实验。假设产品纯碱中只含NaCl、NaHCO3杂质。
(5)检验产品纯碱中是否含有NaCl,可取少量试样溶于水后,再滴加 试剂。
(6)滴定法测定纯碱产品中NaHCO3含量的方法是:准确称取纯碱样品W g,放入锥形瓶中加蒸馏水溶解,加1~2滴酚酞指示剂,用c mol/L的HCl溶液滴定至溶液由红色变为无色(指示CO32- +H+=HCO3-反应的终点),所用HCl溶液体积为V1 mL,再加1~2滴甲基橙指示剂,继续用HCl溶液滴定至溶液由黄色变为橙色,所用HCl溶液总体积为V2 mL。则纯碱样品中NaHCO3质量分数为 。
(1)2NaHCO3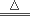 Na2CO3+CO2↑+H2O (3分)
Na2CO3+CO2↑+H2O (3分)
(2)C (2分) (3)D (3分)
(4)饱和NaHCO3溶液 (2分) (5)稀HNO3和AgNO3溶液(2分)
(6)84c(V2- V1)∕1000W (3分)
题目分析:(1)煅烧炉中主要是把沉淀池中得到的NaHCO3加热使之分解得到碳酸钠,方程式为2NaHCO3 Na2CO3+CO2↑+H2O;(2)联合制碱法的生产原料为:食盐、NH3、CO2,A正确;副产物氯化铵可做氮肥,正确;生产过程中可循环利用的物质除CO2外,还有NaCl,错误;联合制碱法最大的优点是使食盐的利用率提高到96%以上,废弃物少,正确。(3)“联合制碱法”的第一步反应为NH3+CO2+H2O+NaCl=NaHCO3↓+NH4Cl,故模拟装置中接口连接顺序为b接c;a接f、e接d;(4)D装置的作用是除去CO2中混有的HCl,可选用饱和NaHCO3溶液;(5)检验产品纯碱中是否含有NaCl,可取少量试样溶于水后,再滴加稀HNO3和AgNO3溶液;(6)根据所给信息可知,样品中NaHCO3的物质的量为c(V2-V1)/1000 mol,故纯碱样品中NaHCO3质量分数为84c(V2- V1)∕1000W。
Na2CO3+CO2↑+H2O;(2)联合制碱法的生产原料为:食盐、NH3、CO2,A正确;副产物氯化铵可做氮肥,正确;生产过程中可循环利用的物质除CO2外,还有NaCl,错误;联合制碱法最大的优点是使食盐的利用率提高到96%以上,废弃物少,正确。(3)“联合制碱法”的第一步反应为NH3+CO2+H2O+NaCl=NaHCO3↓+NH4Cl,故模拟装置中接口连接顺序为b接c;a接f、e接d;(4)D装置的作用是除去CO2中混有的HCl,可选用饱和NaHCO3溶液;(5)检验产品纯碱中是否含有NaCl,可取少量试样溶于水后,再滴加稀HNO3和AgNO3溶液;(6)根据所给信息可知,样品中NaHCO3的物质的量为c(V2-V1)/1000 mol,故纯碱样品中NaHCO3质量分数为84c(V2- V1)∕1000W。
