实验室有四瓶失去标签的溶液,现标为A、B、C、D,分别是碳酸钾溶液、氢氧化钠溶液、硫酸镁溶液和稀盐酸中的一种。
【提出问题】如何区分出四种溶液?
【进行实验】甲同学取少量A溶液于试管中,加入一定量氢氧化钡溶液,观察到无明显现象,由此甲同学认为A一定不是(1) ,甲同学继续向实验后的溶液中滴加酚酞溶液,酚酞溶液由无色变为红色,则甲同学得出结论:A是氢氧化钠溶液。
【表达与交流】乙同学不同意甲同学的结论,乙同学的理由是(2) 。
于是乙同学另取少量A于试管中,向其中滴加一种试剂是(3) 溶液,观察到的明显现象是(4) ,由此证明了甲同学的结论是错误的,同时确定了A。
同学们继续实验:取B、C、D三种溶液置于试管中,分别依次滴加氯化钡溶液和稀硝酸,观察现象。
【收集证据】观察到C中产生白色沉淀,滴加稀硝酸后,沉淀溶解,产生气泡;D中产生白色沉淀,滴加稀硝酸后,沉淀不溶解;B中无明显现象。
【解释与结论】写出D中发生反应的化学方程式(5) 。
同学们最终通过实验区分出了四种溶液。
(1)碳酸钾溶液和硫酸镁溶液
(2)酞溶液由无色变为红色,也可能是由于氢氧化钡溶液过量引起的,所以无法判定溶液一定是氢氧化钠溶液
(3)紫色石蕊
(4)由紫色变为红色
(5)MgSO4+BaCl2=BaSO4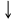 +MgCl2
+MgCl2
题目分析:(1)加入一定量氢氧化钡溶液,观察到无明显现象,氢氧化钠与氢氧化钡不反应,稀盐酸与氢氧化钡反应但无现象,所以溶液一定不是碳酸钾溶液和硫酸镁溶液
(2)实验后的溶液中滴加酚酞溶液,酚酞溶液由无色变为红色,如果是稀盐酸,且氢氧化钡过量也可能有这样的现象,所以原来溶液不一定就是氢氧化钠溶液
(3)(4)甲的结论错误,即A溶液为稀盐酸,检验稀盐酸用紫色石蕊试液,现象溶液由紫色变成红色(5)D中产生白色沉淀,滴加稀硝酸后,沉淀不溶解,则产生的沉淀为硫酸钡沉淀,所以D应该是硫酸镁,反应的方程式为:MgSO4+BaCl2=BaSO4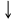 +MgCl2
+MgCl2
