(10分)某粗盐中主要成分为NaCl ,还含有的少量MgCl2、CaCl2和少量泥沙。为了除去杂
质,得到纯净的氯化钠,进行如下实验。
(1)除难溶性杂质。将5g的粗盐溶解于足量水中,需用玻璃棒不断搅拌,目的是 ;进行过滤操作时,需要的玻璃仪器有烧杯、玻璃棒和 ;过滤后,将滤液转移到 (填仪器名称)进行加热蒸发,得到固体精盐4g。若所得精盐的产率偏低,可能的原因是 (填字母)。
A.部分粗盐未溶解 B.蒸发时未使用玻璃棒进行搅拌,导致液滴飞溅 C. 过滤时,滤纸破损了
(2)除可溶性杂质。经过上述操作后,精盐中仍存在少量的MgCl2、CaCl2未除去,现设计如下实验进行提纯,提纯的流程如下:
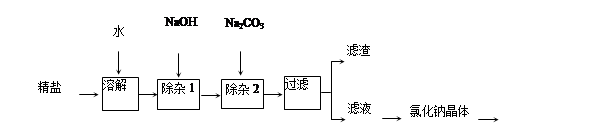
回答下列问题:
①用NaOH为了除去MgCl2杂质,反应的化学方程式为____________________ _。
②NaOH和Na2CO3如果添加过量了,需往滤液中加入适量___________除去。
③过滤后,所得滤渣中含有的物质是 (填化学式)。
④从滤液中得到氯化钠固体的主要操作是蒸发,为了获得纯净的氯化钠,应蒸发至__ _(填序号)。
A.完全蒸干时停止加热 B.快干时停止加热,利用余热蒸干
(1)加快溶质溶解速率(充分溶解);漏斗;蒸发皿; AB;(2)①2NaOH+MgCl2===Mg(OH)2↓+2NaCl;
②稀HCl; ③ Mg(OH)2、CaCO3;④ B。
题目分析:(1)溶解玻璃棒搅拌是为了加速溶解,过滤要用到的玻璃仪器有烧杯、漏斗和玻璃棒;蒸发皿用于蒸发结晶,粗盐的产率就是所得氯化钠的质量比上粗盐的质量,A部分粗盐未溶解;B.蒸发时未使用玻璃棒进行搅拌,导致液滴飞溅;都会使得到的食盐质量偏小;C滤纸破损需再过滤不会影响得到的氯化钠的质量;(2)①氯化镁和氢氧化钠反应生成氢氧化镁沉淀和氯化钠,反应的化学方程式为:2NaOH+MgCl2═Mg(OH)2↓+2NaCl;②氢氧化钠和碳酸钠都能和稀盐酸反应生成氯化钠,并且过量的稀盐酸加热会挥发;
③氯化镁和氢氧化钠反应生成氢氧化镁沉淀和氯化钠,碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠;
④蒸发结晶要等到蒸发皿中出现较多晶体就停止加热利用余热将水分蒸干,不能完全蒸干再停止加热。
