问题
选择题
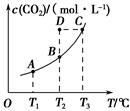
一定条件下,向容积为2 L的密闭容器中充入1 mol CO2和3 mol H2,发生如下反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),5 min后反应达到平衡时c(CH3OH)为0.2 mol·L-1。CO2(g)的平衡物质的量浓度c(CO2)与温度关系如图所示。下列说法错误的是( )。
CH3OH(g)+H2O(g),5 min后反应达到平衡时c(CH3OH)为0.2 mol·L-1。CO2(g)的平衡物质的量浓度c(CO2)与温度关系如图所示。下列说法错误的是( )。
A.0~5 min,CO2的平均反应速率为0.04 mol·(L·min)-1
B.反应CO2(g)+3H2(g) CH3OH(g)+H2O(g)的ΔH<0
CH3OH(g)+H2O(g)的ΔH<0
C.在T2℃时,若反应处于状态D,则一定有v正<v逆
D.若T1℃、T2℃时的平衡常数分别为K1、K2,则K1>K2
答案
答案:C
由反应方程式可知,5 min后CO2转化了0.4 mol,则0~5 min,CO2的平均反应速率为0.04 mol·(L·min)-1,A正确。从图像可以看出,温度升高,c(CO2)增大,说明正反应是放热反应,B正确。在T2℃时,若反应处于状态B,则是平衡状态,由D→B反应正向进行,一定有v正>v逆,C错误。因为该正反应的ΔH<0,所以温度升高时平衡逆向移动,平衡常数减小,故K1>K2,D正确。
