问题
推断题
根据下列框图关系填空,已知反应①、③是工业生产中的重要反应,D、E常温下为气体、X常温下为无色液体,H与E相对分子质量之间的关系为:Mr(H)-Mr(E)=34,又知C焰色反应通过蓝色钴玻璃火焰呈紫色。
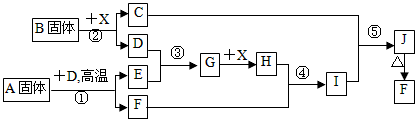
(1)固体B的电子式为_______________,其中所包含的化学键有_______________。
(2)固体A的化学式为_______________,其中非金属元素的化合价为_______________。
(3)反应④的离子方程式_________________________。反应⑤的化学方程式_____________________。
(4)用铜作电极电解H溶液,阳极的电极反应式是_________________________。
(5)若生成16gE,放出106.5kJ热量,则1mol A与足量D反应放出热量为:____________kJ。
答案
(1)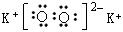 ;离子键、共价键(或非极性键)
;离子键、共价键(或非极性键)
(2)FeS2;-1
(3)Fe2O3+6H+==2Fe3++3H2O;Fe2(SO4)3+6KOH=2Fe(OH)3↓+3K2SO4
(4)Cu-2e=Cu2+
(5)852
