问题
推断题
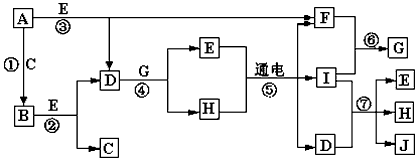
A-J是中学化学中常见的几种物质,它们之间的转化关系如图所示。已知常温下A为固体单质,B为淡黄色粉末,C、F、I为气态单质,E在常温下为液体,且E可由C、F合成,J可用作杀菌消毒剂。回答下列问题
(1)B中的化学键有________(填“离子键”、“极性键”或“非极性键”) E的电子式________。
(2)写出反应⑦的离子方程式 __________________________。
(3)向AlCl3溶液中加入少量固体B,写出反应的化学方程式_____________________。
(4)常温下1克F单质在足量C单质中燃烧生成稳定的液态物质E释放出142.9kJ热量,写出液态E分解的热化学方程式________________。
(5)以Pt为电极电解滴加有少量酚酞的H饱和溶液,则在________(填“阴或阳”)极附近溶液由无色变为红色,其原因是________________。
答案
(1)离子键、非极性键;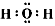
(2)Cl2+2OH-=Cl-+ClO-+H2O
(3)4AlCl3+6Na2O2+6H2O=4Al(OH)3↓+12NaCl+3O2↑
(4)H2O(l) = H2(g) +1/2O2(g) △H=+285.8kJ/mol
(5)阴极;在阴极由于H+得到电子产生H2,破坏了水的电离平衡,促进水继续电离,导致溶液中
c(OH-)>c(H+),溶液呈碱性,所以阴极附近溶液变为红色
