下图所示各物质是由1~20号元素中部分元素组成的单质或其化合物,图中部分反应条件未列出。已知C、H是无色有刺激性气味的气体,D是一种黄绿色的气体单质,物质J可用于泳池消毒。反应②和④是化工生产中重要反应,反应⑤是实验室制备气体C的重要方法。
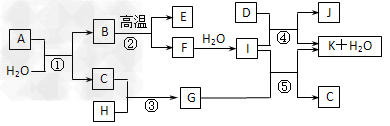
请回答下列问题:
(1)物质E的电子式是__________;I中所含化学键类型为:____________________;气体D所含元素在周期表中的位置是____________________。
(2)G的水溶液呈__________性,用离子方程式表示其原因___________________________。
(3)写出E与过量I溶液反应原离子方程式______________________________。
(4)写出实验室制备气体C反应的化学方程式______________________________,干燥气体C可选用__________做干燥剂(填名称)。
(5)写出反应④的化学方程式_________________________________。
(6)反应③的现象为______________________________。
(7)已知含7.4g I的稀溶液与200mL 1 mol/L的H溶液反应放出11.56kJ的热量,写出该反应的热化学方程式________________________________________。
(8)物质A由三种元素组成,1 molA与水反应可生成1 mol B和2 mol C,A化学式为______________________________。
(1)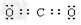 ;离子键、极性键;第三周期VIIA族
;离子键、极性键;第三周期VIIA族
(2)酸;NH4++H2O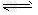 NH3·H2O+H+
NH3·H2O+H+
(3)CO2+Ca2++2OH-=CaCO3↓+H2O
(4)2NH4Cl+Ca(OH)2===CaCl2+2NH3↑+2H2O;碱石灰
(5)2Cl2+2Ca(OH)2===CaCl2+Ca(ClO)2+2H2O
(6)大量白烟
(7)Ca(OH)2(aq)+2HCl(aq)===CaCl2(aq)+2H2O(l) △H=-115.6kg/mol
(8)CaCN2
