A、B、C、X均为常见的纯净物,它们之间有如下转化关系(副产品已略去).
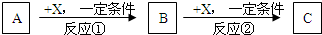
试回答:
(1)若X是强氧化性单质,则A不可能是______.
a.S b.N2 c.Na d.Mg e.Al
(2)若X是金属单质,向C的水溶液中滴入AgNO3溶液,产生不溶于稀HNO3的白色沉淀,则B的化学式为______;C溶液在贮存时应加入少量X,理由是(用必要的文字和离子方程式表示)______.检验此C溶液中金属元素价态的操作方法是______.
(3)若A、B、C为含某金属元素的无机化合物,X为强电解质,A溶液与C溶液反应生成B,则B的化学式为______,X的化学式可能为(写出不同类物质)______或______.反应①的离子方程式为______.
(1)若X是强氧化性单质,由转化关系A
BX
C知,A、B、C中含有的相同元素必须是变价元素,X
a.S和氧气反应生成二氧化硫,二氧化硫和氧气反应生成三氧化硫,符合转化关系A
BX
C,故不选;X
b.N2 和氧气反应生成一氧化氮,一氧化氮和氧气反应生成二氧化氮,符合转化关系A
BX
C,故不选;X
c.Na和氧气反应生成氧化钠,氧化钠和氧气反应生成过氧化钠,符合转化关系A
BX
C,故不选;X
d.Mg和氧气反应生成氧化镁,氧化镁和氧气不反应,所以不符合转化关系A
BX
C,故选;X
e.Al和氧气反应生成氧化铝,氧化铝和氧气不反应,所以不符合转化关系A
BX
C,故选;X
故选d、e;
(2)向C的水溶液中滴入AgNO3溶液,产生不溶于稀HNO3的白色沉淀,则C中含有氯离子,若X是一种金属单质,由转化关系A
BX
C,X为变价金属铁,A为强氧化性物质,根据元素守恒知,A是氯气,B是氯化铁,C是氯化亚铁;X
贮存氯化亚铁溶液时,亚铁离子易被氧气氧化生成铁离子,为防止亚铁离子被氧化且不引进新的杂质,应该向氯化亚铁溶液中加入铁粉;
亚铁离子和硫氰化钾溶液不反应,铁离子和硫氰化钾溶液混合溶液呈红色,此现象是铁离子的特征反应,所以检验是否含有铁离子的方法是:向溶液中滴加少量KSCN溶液,无明显现象,通入少量Cl2溶液呈血红色;
故答案为:FeCl3; 2Fe3++Fe═3Fe2+,保证溶液中Fe2+为主;向溶液中滴加少量KSCN溶液,无明显现象,通入少量Cl2溶液呈血红色;
(3)若A、B、C为含某金属元素的无机化合物,X为强电解质,由转化关系A
BX
C,且A+C→B,考虑Al的化合物的相互转化,X
若X是一种强碱,A为铝盐,B为Al(OH)3,C为偏铝酸盐;
若X是一种强酸,A为偏铝酸盐,B为Al(OH)3,C为铝盐;
通过以上分析知,B是Al(OH)3,X是HCl或NaOH,偏铝酸盐和酸反应生成氢氧化铝沉淀,铝盐和碱反应生成氢氧化铝沉淀,离子方程式为:AlO2-+H++H2O═Al(OH)3↓或Al3++3OH-═Al(OH)3↓;
故答案为:Al(OH)3;HCl或NaOH;AlO2-+H++H2O═Al(OH)3↓或Al3++3OH-═Al(OH)3↓.
