今年3月22日是第二十个“世界水日”,它的主题是“水与粮食安全”.关于水的知识有下列问题,请按要求填空:
(1)除去水样中难溶性的固体,需将水样(填序号)______;
①加热 ②过滤 ③蒸发 ④冷却
(2)有关水的组成和结构的叙述中,正确的是______ (填字母);
A.水中氢、氧元素的质量比为2:1
B.水是由水分子构成的
C.水分子是由氢分子和氧原子构成的
(3)欲除去水中不溶性杂质,需进行过滤操作,该操作过程中玻璃棒所起的作用是______.
(4)生活中为降低水的硬度并杀灭水中病原生物,可采用的方法是______.
(5)某同学在完成电解水实验时,发现正极产生了10mL气体,则负极产生的气体体积是______.该实验能够说明水是由氢元素与氧元素组成的理论依据是______.
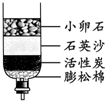
(6)用如图所示的简易净水器处理浑浊的河水,下面分析正确的是______
A.净水器能杀菌消毒
B.净化后的水属于纯净物
C.活性炭的主要作用是吸附
D.净水器能将硬水变为软水
(7)下列节水措施中不可取的是______
A.工业废水处理达标后循环使用
B.农业浇灌推广使用喷灌、滴灌技术
C.大量开采使用地下水
D.洗菜、淘米、洗衣的水可以用来浇花、拖地、冲厕所.
(1)过滤是除去水中不溶性固体杂质的方法,故填:②;
(2)A、水中氢元素与氧元素的质量比为1×2:16=1:8,故A错误;
B、水是由水分子构成的,故B正确;
C、水分子是由氢原子和氧原子构成的,故C错误;
故填:B;
(3)过滤操作中玻璃棒起到了引流的作用,故填:引流;
(4)硬水中含有较多的可溶性钙镁化合物,受热可以转化为不溶性钙镁化合物,故可以使用加热的方法降低水的硬度,同时加热能杀死水中含有的细菌微生物,故填:加热煮沸;
(5)电解水时生成的氢气和氧气的体积比为2:1,正极产生的氧气为10mL,则负极生成的氢气的体积为20mL,根据质量守恒定律,化学反应前后元素的种类不变,故该实验说明水是由氢氧元素组成的,故填:20mL,质量守恒定律;
(6)A、简易净水器不能杀死细菌,故A错误;
B、通过简易净水器处理得到的水中含有其他杂质,不是纯净物,故B错误;
C、活性炭具有吸附性,能吸附色素和异味,该净水器中主要利用活性炭的吸附作用,故C正确;
D、该净水器不能除去水中含有的可溶性钙镁化合物,不能将硬水软化,故D错误;
故填:C;
(7)A、工业废水处理达标后循环使用,能起到节约水资源的作用;
B、农业浇灌推广使用喷灌、滴灌技术,能起到节约用水的作用;
C、大量开采使用地下水,不利于保护水资源;
D、洗菜、淘米、洗衣的水可以用来浇花、拖地、冲厕所可以节约用水;
故填:C.
