有A、B、C、D、E、F、G、H等常见物质,已知有如下图转化关系,其中B、C 为常见非金属单质;F为常见金属单质;B在C中燃烧时,火焰呈苍白色;A和D的焰色反应为黄色.G和D溶液混和,产生红褐色沉淀.
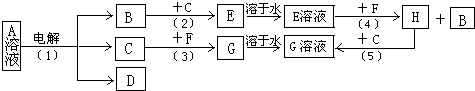
(1)反应(1)中若生成0.1mol B,则转移的电子的物质的量为______.写出C与F反应的化学方程式______.(注明反应条件)
(2)图中所示的5个反应中属于氧化还原反应的有:______.(填写编号)
(1)B在C中燃烧时,火焰呈苍白色,说明B是H2,C是Cl2,则E是HCl气体,E溶液为盐酸.A和D的焰色反应为黄色,说明A和D中含Na+.G和D溶液混和,产生红褐色沉淀,为Fe(OH)3沉淀,说明G中含Fe3+,结合F为常见金属单质,推得F为金属Fe.反应(3)为Cl2和Fe反应生成FeCl3,反应(4)为盐酸和Fe反应生成FeCl2和H2,反应(5)为FeCl2和Cl2反应生成FeCl3.B是H2,C是Cl2,D中含Na+,根据电解原理推得反应(1)是电解饱和食盐水,即A溶液为NaCl溶液.反应(1)方程式为:2NaCl+2H2O═2NaOH+H2↑+Cl2↑,生成1molH2转移2mol电子,则生成0.1molH2,转移的电子的物质的量为0.2mol,C与F反应的化学方程式为:2Fe+3Cl2
2FeCl3, 点燃 .
故答案为:0.2mol;2Fe+3Cl2
2FeCl3; 点燃 .
(2)反应(1)方程式为:2NaCl+2H2O
2NaOH+H2↑+Cl2↑, 电解 .
反应(2)方程式为:H2+Cl2
2HCl, 点燃 .
反应(3)方程式为:2Fe+3Cl2
2FeCl3, 点燃 .
反应(4)方程式为:2HCl+Fe═FeCl2+H2↑,
反应(5)方程式为:2FeCl2+Cl2═2FeCl3.
上述5个反应中都有化合价的变化,所以都属于氧化还原反应.
故答案为:(1)、(2)、(3)、(4)、(5).
