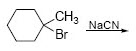
T℃时,在一个体积为2L的容器中,A气体与B气体反应生成C气体,反应过程中A、B、C浓度变化如图所示.
(1)写出该反应的方程式:______
(2)计算该温度下该反应的平衡常数:______
(3)已知:K(300℃)>K(350℃),该反应是______热反应.
(4)0~4分钟时,A的平均反应速率为:______
(5)到达平衡时B的转化率为:______
(6)恒容条件下,下列措施中能使n(A)/n(C)降低的有______.
A.充入氦气 B.使用催化剂
C.再充入2.4molA和1.6molB D.降低温度.
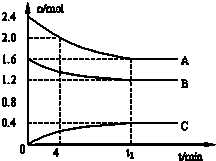
(1)由图象可以看出,反应中A、B的物质的量减小,C的物质的量增多,则A、B为反应物,C为生成物,
且△n(A):△n(B):△n(C)=0.8mol:0.4mol:0.4mol=2:1:1,则反应的化学方程式为:2A+B
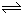
C,
故答案为:2A+B
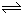
C;
(2)k=
=c(C) c2(A)•c(B)
=0.52(mol/L)-2,故答案为:0.52;0.2mol/L (0.8mol/L)2•0.6mol/L
(3)K(300℃)>K(350℃),说明温度升高,平衡向逆反应方向移动,则正反应为放热反应,故答案为:放;
(4)0~4分钟时,A的平均反应速率为:v(A)=
=0.05mol•L-1•min-1,故答案为:0.05mol•L-1•min-1;2.4mol-2.0mol 2L 4min
(5)到达平衡时B的转化率为:
×100%=25%,故答案为:25%;1.6mol-1.2mol 1.6mol
(6)
降低,说明平衡向正反应方向移动:n(A) n(C)
A.充入氦气,各物质的物质的量浓度不变,平衡不移动,故A错误;
B.使用催化剂,平衡不移动,故B错误;
C.再充入2.4molA和1.6molB,反应物的浓度增大,平衡向正反应方向移动,故C正确;
D.降低温度,平衡向正反应方向移动,故D正确,
故答案为:CD.