各物质之间的转化关系如下图,部分生成物省略.C、D是由X、Y、Z中两种元素组成的化合物,X、Y、Z的原子序数依次增大,在周期表中X的原子半径最小,Y、Z原子最外层电子数之和为10.D为无色非可燃性气体,G为黄绿色单质气体,J、M为金属,I有漂白作用,反应①常用于制作印刷电路板.
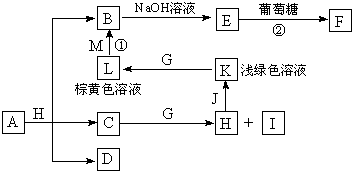
请回答下列问题:
(1)写出A的化学式______,C的电子式______.
(2)比较Y与Z的原子半径大小:______>______(填写元素符号).
(3)写出反应②的化学方程式(有机物用结构简式表示)______,
举出该反应的一个应用实例______.
(4)已知F溶于稀硝酸,溶液变成蓝色,放出无色气体.请写出该反应的化学方程式______.
(5)研究表明:气体D在一定条件下可被还原为晶莹透明的晶体N,其结构中原子的排列为正四面体,请写出N及其2种同素异形体的名称______、______、______.
(1)X在周期表中的原子半径最小,为H;“C(H2O)、D由X(H)、Y、Z中两种元素组成”,则Y、Z中有氧(O),再结合“Y、Z原子最外层电子数之和为10”、“X、Y、Z的原子序数依次增大”,可以确定Z为氧(O)、Y为碳(C).进而推出D(由H、C、O中的两种元素组成;无色非可燃性气体)为CO2.最后,从A+H(HCl)=B(CuCl2)+C(H2O)+D(CO2)可知,A是含有Cu2+的碳酸盐,所以A是CuCO3或Cu2(OH)2CO3;C为H2O;水的电子式为:
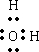
;
故答案为:CuCO3或Cu2(OH)2CO3
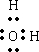
;
(2)Y与Z分别是C、O,依据铜周期原子半径依次减小判断,C、O的原子半径C>O;故答案为:C O;
(3)依据判断可知,反应②是葡萄糖和氢氧化铜加热反应,反应的化学方程式为:CH2OH(CHOH)4CHO+2Cu(OH)2
CH2OH(CHOH)4COOH+Cu2O↓+2H2O;加热
故答案为:CH2OH(CHOH)4CHO+2Cu(OH)2
CH2OH(CHOH)4COOH+Cu2O↓+2H2O;加热
(4)F(Cu2O)+HNO3 Cu(NO3)2(从蓝色可确定为Cu2+)+NO(从无色气体可以确定),然后根据化合价升降法配平即可,反应的化学方程式为:3Cu2O+14HNO3=6Cu(NO3)2+2NO↑+7H2O;
故答案为:3Cu2O+14HNO3=6Cu(NO3)2+2NO↑+7H2O;
(5)CO2可以还原成正四面体结构的晶体N,即化合价降低,显然生成了金刚石,它的同素异形体必须为含碳的单质,同素异形体的名称为:金刚石、如石墨、富勒烯(C60);
故答案为:金刚石、如石墨、富勒烯(C60);
