各物质之间的转化关系如图,部分生成物省略.C、D是由X、Y、Z中两种元素组成的化合物,X、Y、Z的原子序数依次增大,在周期表中X的原子半径最小,Y、Z原子最外层电子数之和为10.D为无色非可燃性气体,G为黄绿色单质气体,J、M为金属,I有漂白作用,反应①常用于制作印刷电路板.
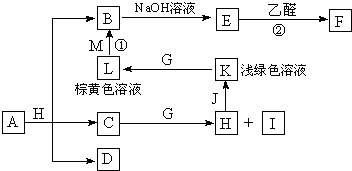
据此回答下列各题:
(1)写出纯净物A的化学式______,C的电子式______,用来检验L中阳离子的试剂是______(该试剂焰色为紫色).
(2)沉淀E可溶于过量______(填试剂名称)得到深蓝色的透明溶液,呈现该颜色是因为溶液中存在配离子______(填化学式).
(3)写出反应①的离子方程式______,写出反应②的化学方程式(有机物用结构简式表示)______.
(4)已知F溶于稀硝酸,溶液变成蓝色,放出无色气体,请写出该反应的化学方程式______.
X在周期表中的原子半径最小,为H元素,Y、Z原子最外层电子数之和为10,“X、Y、Z的原子序数依次增大”,进而推出D(由H、C、O中的两种元素组成;无色非可燃性气体)为CO2,可以知道X、Y、Z是H、C、O,则C为H2O,H为HCl,I有漂白作用,应为HClO,浅绿色、棕黄色溶液为Fe2+和Fe3+,可知J为Fe,K为FeCl2,L为FeCl3,反应①用于制作印刷电路板为FeCl3和Cu,则M为Cu,B为CuCl2,E能与乙醛反应,应为Cu(OH)2,F为Cu2O,从A+H(HCl)=B(CuCl2)+C(H2O)+D(CO2)可知,A是含有Cu2+的碳酸盐,从A+H(HCl)=B(CuCl2)+C(H2O)+D(CO2)可知,A是含有Cu2+的碳酸盐,应为CuCO3或Cu2(OH)2CO3或Cu(OH)2?CuCO3,
(1)由以上分析可知A是CuCO3或Cu2(OH)2CO3或Cu(OH)2?CuCO3,C为H2O,电子式为
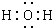
,L为FeCl3,用来检验L中阳离子的试剂是硫氰化钾,
故答案为:CuCO3或Cu2(OH)2CO3或Cu(OH)2?CuCO3;
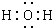
;硫氰化钾;
(2)E为Cu(OH)2,可与氨水发生络合反应生成[Cu(NH3)4]2+,得到深蓝色的透明溶液,
故答案为:氨水;[Cu(NH3)4]2+;
(3)反应①为氯化铁和铜的反应,反应的离子方程式为Cu+2Fe3+═Cu2++2Fe2+,乙醛和氢氧化铜浊液在加热的条件下反应的方程式为CH3CHO+2Cu(OH)2+NaOH
CH3COONa+Cu2O↓+3H2O,△
故答案为:Cu+2Fe3+═Cu2++2Fe2+;CH3CHO+2Cu(OH)2+NaOH
CH3COONa+Cu2O↓+3H2O;△
(4)F为Cu2O,与稀硝酸反应生成硝酸铜和NO,反应的化学方程式为3Cu2O+14HNO3=6Cu(NO3)2+2NO+7H2O,
故答案为:3Cu2O+14HNO3=6Cu(NO3)2+2NO+7H2O.
