如图是部分短周期元素的单质及其化合物的转化关系图(有关反应的条件及生成的H2O已略去).已知:
(a)A、B、C、D都是非金属单质,其中B、C、D在常温常压下是气体.
(b)反应①、②是化工生产中的重要反应.
(c)化合物E是形成酸雨的污染物之一,化合物K是常用的氮肥.
(d)化合物L具有漂白性,可由Cl2与NaOH溶液反应而制得.
(e)化合物J由两种元素组成,它是火箭推进剂的成分之一,其相对分子质量为32.
请按要求填空:
(1)反应③的化学方程式______.
(2)C的结构式______;H的化学式______.
(3)L的溶液与化合物E反应的离子方程式:______.
(4)化合物J的化学式______.
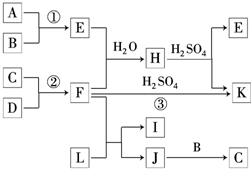
由短周期元素的单质及其化合物的转化关系图可知,化合物E是形成酸雨的污染物之一,则E为SO2,A、B、C、D都是非金属单质,其中B、C、D在常温常压下是气体,则A为S,B为O2;化合物K是常用的氮肥,K为硫酸铵,所以F为氨气,则C、D分别为N2、H2;化合物L具有漂白性,可由Cl2与NaOH溶液反应而制得,则L为NaClO,氨气与NaClO反应生成J,J由两种元素组成,它是火箭推进剂的成分之一,其相对分子质量为32,则J为N2H4;J与氧气反应生成C,C为氮气,
(1)该反应为氨气与硫酸反应生成硫酸铵,化学反应为2NH3+H2SO4═(NH4)2SO4,
故答案为:2NH3+H2SO4═(NH4)2SO4;
(2)C为氮气,其结构式为N≡N,H为二氧化硫与氨气在水中的反应,反应生成(NH4)2SO3或NH4HSO3,故答案为:N≡N;(NH4)2SO3或NH4HSO3;
(3)L为NaClO,E为SO2,在溶液中发生氧化还原反应生成氯化钠、硫酸钠,离子反应为ClO-+SO2+2OH-═Cl-+SO42-+H2O或ClO-+SO2+H2O═Cl-+SO42-+2H+,
故答案为:ClO-+SO2+2OH-═Cl-+SO42-+H2O或ClO-+SO2+H2O═Cl-+SO42-+2H+;
(4)由上述推断可知,J为N2H4,故答案为:N2H4.
