A、B、C、X是中学化学1中常见的4种物质,它们均由短周期元素组成,转化关系如图所示.请针对以下两种情况1回答下列问题:
(1)若A、B、C中均含同一种常见金属元素,该元素在C中以阴离子形式存在.将A、C的水溶液混合可得白色胶状沉淀B.
①A中含有的金属元素为______(填元素名称).
②该金属元素的单质与某氧化物在高温下反应,可用于焊接铁轨及定向爆破,此反应的化学方程式为______.
(2)若A、B、C的焰色反应均呈黄色,水溶液均呈碱性.
①A中所含有的化学键是______、______.
②将4.48L(标准状况下)X通入100mL 3mol•L-1A的水溶液后,溶液中离子浓度由大到小的顺序为______.
③自然界中存在由B或C与H2O按一定比例结晶而成的固体.将一定量的由C与H2O按一定比例形成的晶体溶于水配制成100mL溶液,测得溶液中金属阳离子的浓度为0.5mol•L-1.若取相同质量的此晶体加热至恒重,剩余固体的质量为______.
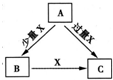
A、B、C、X是中学化学常见物质,均由短周期元素组成,则
(1)若A、B、C中均含同一种常见金属元素,将A、C的水溶液混合可得B的沉淀,由转化关系可知,A含有铝离子,B为氢氧化铝,C含有偏铝酸根,X为氢氧化钠,
①由上述分析可知A、B、C中含有的同一种常见金属元素为Al,名称为铝,故答案为:铝;
②Al与氧化铁发生铝热反应可用于焊接铁轨及定向爆破,此反应的化学方程式为2Al+Fe2O3
Al2O3+2Fe,故答案为:2Al+Fe2O3 高温 .
Al2O3+2Fe; 高温 .
(3)若A、B、C的焰色反应均呈黄色,水溶液均为碱性;将C加到盐酸中,有无色无味的气体X产生,则A为氢氧化钠,B为碳酸钠,C为碳酸氢钠,X为二氧化碳,
①A为氢氧化钠,属于离子化合物,钠离子与氢氧根离子之间形成离子键,氢氧根离子中氧原子与氢原子之间形成1对共用电子对,为共价键,属于A中所含有的化学键是离子键、共价键,故答案为:离子键;共价键.
②X为二氧化碳,将4.48L(标准状况下)X通入100mL 3mol•L-1A的水溶液后,n(CO2)=0.2mol,n(NaOH)=0.3mol,反应的为3NaOH+2CO2=Na2CO3+NaHCO3+H2O,即反应后溶液中存在等量的Na2CO3、NaHCO3,溶液因水解显碱性,碳酸根离子水解大于碳酸氢根离子的水解,则溶液中离子浓度由大到小的顺序为c(Na+)>c(HCO3-)>
c(CO32-)>c(OH-)>c(H+),故答案为:c(Na+)>c(HCO3-)>c(CO32-)>c(OH-)>c(H+);
③自然界中存在B、C和H2O按一定比例结晶而成的固体.取一定量该固体溶于水配成100mL溶液,测得溶溶中金属阳离子的浓度为0.5mol/L,即钠离子浓度为0.5mol/L.取相同质量的固体加热至恒重,剩余固体为碳酸钠,根据钠离子守恒可知,碳酸钠的质量为
×0.1L×0.5mol/L×106g/mol=2.65g.1 2
故答案为:2.65g.

