已知物质M由同一短周期的X、Y两种元素组成,X原子的最外层电子数是最内层电子数的一半,Y元素最高正价与它的负价代数和为6.M与其他物质的转化关系如图(部分产物已略去):
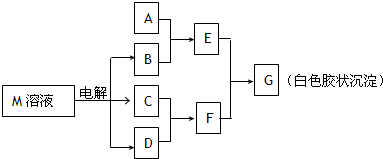
(1)若A是与X、Y同周期的一种常见金属,则A元素在周期表中的位置是______周期______族,写出A与B溶液反应的化学方程式______.
(2)若A是某元素的一种常见酸性氧化物,可用于制造光导纤维,则该元素原子结构示意图为______,写出E与F反应的离子方程式______.
(3)B的电子式为______,其中的化学键为______.用电子式表示M的形成过程______.
(4)工业上用电解物质M的产物之一氧化有毒含氰(CN-)碱性废水,得到无毒的N2、CO2等.写出此反应的离子反应方程式______.
X原子的最外层电子数是最内层电子数的一半,则X是Na元素,X和Y属于同一周期,且Y元素最高正价与它的负价代数和为6,则Y是Cl元素,物质M由同一短周期的X、Y两种元素组成,则M是NaCl,电解氯化钠溶液生成氢气、氯气和氢氧化钠,
(1)若A是与X、Y同周期的一种常见金属,则A是铝,铝能和氢氧化钠反应,则B是氢氧化钠,铝在元素周期表中位于第三周期第IIIA族,铝和氢氧化钠溶液反应生成偏铝酸钠和氢气,其反应方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,
故答案为:第三;IIIA族;2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
(2)若A是某元素的一种常见酸性氧化物,可用于制造光导纤维,则A是二氧化硅,所以该元素是硅元素,二氧化硅能和B溶液反应生成E,则B是氢氧化钠溶液,二氧化硅和氢氧化钠溶液生成E硅酸钠,氯气和氢气反应生成F氯化氢,硅酸钠和盐酸反应生成G硅酸,硅原子核外有14个电子,其原子结构示意图为:
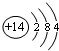
,盐酸和硅酸钠反应生成硅酸的离子反应方程式为:2H++SiO32-=H2SiO3↓,
故答案为:
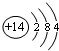
;2H++SiO32-=H2SiO3↓;
(3)B是氢氧化钠,其电子式为:
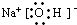
; 氢氧化钠中钠离子和氢氧根离子之间存在离子键,氢原子和氧原子之间存在共价键,氯化钠的形成过程中钠原子失电子,氯原子得电子,所以氯化钠的形成过程为:

,
故答案为:
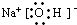
;离子键和共价键;

;
(4)氯气氧化氰(CN-)生成N2、CO2,自身被还原生成氯离子,其离子反应方程式为:5Cl2+2CN-+8OH-=10Cl-+N2+2CO2+4H2O,故答案为:5Cl2+2CN-+8OH-=10Cl-+N2+2CO2+4H2O.

