“暖足贴”利用铁氧化生锈时会放热的原理从而达到给人局部热敷的作用,具有一贴即热,快速热敷的作用,深受大众的喜爱.下图甲是某品牌“暖足贴”的图片.A、B两小组的同学,通过查阅资料发现,其主要成份为:铁粉、活性炭、水、食盐等物质.
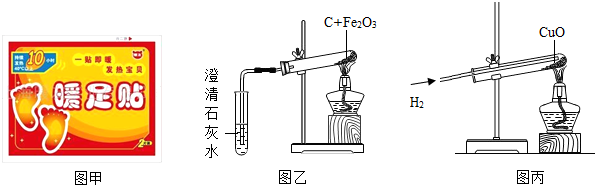
(1)发热剂需接触到空气才会发热,原因是铁要与______、______ 等物质共同作用才会生锈,铁生锈发生氧化反应,放出热量.
(2)试推测发热剂成分氯化钠的作用是______,从而更快的放出热量;“暖足贴”的发热还应用了活性炭具有______性.
(3)打开用过的“暖足贴”,兴趣小组的同学们发现原先黑色的铁粉颜色变成了红棕色.他们想到了金属的回收及利用的重要性,考虑能否用学过的知识将之还原成铁粉.于是,他们在实验室找来炭粉及Fe2O3粉末,在做完图乙所示实验后,发现澄清石灰水变浑浊,试管中粉末全部变为黑色.A组一同学将黑色粉末倒在纸上,发现纸竟然烧起来了,原因是______;另一同学立即用一块湿抹布进行扑盖,火马上熄灭,试说明灭火原理______
(4)B组同学在正确操作之后,取少量黑色粉末,加入足量稀硫酸充分振荡,但她惊讶地发现黑色粉末没有溶解,试管中也未产生预期的气泡,这说明该反应并没有生成______.
(5)A、B组同学查阅资料,得到关于铁的氧化物相关信息如下:
| 铁的氧化物 | Fe2O3 | Fe3O4 | FeO |
| 颜色 | 红色 | 黑色 | 黑色 |
| 化学性质 | 可溶于稀硫酸 | 常温下不溶于稀硫酸 | 可溶于稀硫酸 |
(6)两组同学联想到还原性气体H2,通过继续查阅资料发现酒精灯火焰的温度在600℃左右,而H2还原氧化铜所需温度大约在250℃,他们按图丙所示进行实验,看到了预期现象,写出试管中反应的方程式______.
(1)根据铁制品锈蚀的过程,实际上是铁与空气中的氧气,水蒸气等发生化学反应的过程,因此发热剂需接触到空气才会发热,原因是铁要与 水、氧气等物质共同作用才会生锈.
故答案为:水;氧气;
(2)发热剂成分中氯化钠的作用是加速铁粉生锈,更快放出热量;“暖足贴”的发热还应用了活性炭的吸附作用.
故答案为:加快铁的生锈;吸附;
(3)未等黑色粉末冷却便倒出,致使纸的温度达到了着火点,所以将黑色粉末倒在纸上,发现纸竟然烧起来了;用一块湿抹布进行扑盖,使纸隔绝空气而灭火;
故答案为:未等黑色粉末冷却便倒出,致使纸的温度达到了着火点;隔绝空气;
(4)乙实验完成后,发现澄清石灰水变浑浊,生成部分黑色粉末,黑色粉末是Fe3O4,从题中信息看Fe3O4常温下不溶于稀酸,所以黑色粉末没有溶解,试管中也未产生预期的气泡,说明反应没有发生,无铁单质生成.
故答案为:铁;
(5)根据以上信息,图乙实验中炭粉与Fe2O3发生反应的化学方程式是C+6Fe2O3
CO2+4Fe3O4; 高温 .
故答案为:C+6Fe2O3
CO2+4Fe3O4; 高温 .
(6)氢气还原氧化铜的化学方程式是H2+CuO
Cu+H2O; △ .
故答案为:H2+CuO
Cu+H2O. △ .
