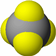
4种短周期元素A、B、C、D的相关信息如下:信息①原子半径大小:A>B>C>D信息②4种元素的原子之间形成的甲、乙和丙3种物质的部分信息如下:
| 甲 | 乙 | 丙 | |
| 分子 比例模型 |
|
|
|
| 物质性质 | 地球上最常见的物质,是组成生物体的重要物质之一,约占人体质量的2/3. | 无色,无气味并且易燃.是常见的一种基础能源. | 有强氧化性的弱酸,可以用于消毒杀菌. |
(1)元素B在周期表中的位置______,丙分子的电子式______.
(2)元素E、F与元素A处于同一周期,E单质的还原性最强,且与甲能反应生成化合物X.含元素F的某些盐可作为净水剂,由元素F、C组成的化合物Y可作为耐火材料.
①写出元素A的单质与甲反应的化学方程式:______.
②写出化合物Y溶解于X溶液的离子方程式:______.
甲是地球上最常见的物质,是组成生物体的重要物质之一,约占人体质量的
,则甲应为H2O,组成元素为H和O,2 3
乙是无色,无气味并且易燃.是常见的一种基础能源,由比例模型可知乙为CH4,组合成元素为C和H,
丙是有强氧化性的弱酸,可以用于消毒杀菌,由比例模型可知丙为HClO,含有元素为H、Cl、O,
原子半径Cl>C>O>H,结合原子半径大小:A>B>C>D,可是A为Cl,B为C,C为O,D为H,则
(1)B为C,原子序数为6,原子核外有2个电子层,最外层电子数为4,则位于周期表第2周期IVA族,
丙为HClO,电子式为

,
故答案为:第2周期IVA族;

;
(2)元素E、F与元素A(即Cl)处于同一周期,E单质的还原性最强,应为Na,且与甲(即H2O)能反应生成化合物X,应为NaOH,含元素F的某些盐可作为净水剂,由元素F、C组成的化合物Y可作为耐火材料,应为Al2O3,则F为Al,
①Cl2和H2O反应的化学方程式为Cl2+H2O=HCl+HClO,
故答案为:Cl2+H2O=HCl+HClO;
②化合物Y为Al2O3,X为NaOH,二者反应的离子方程式为Al2O3+2OH-=2AlO2-+H2O,
故答案为:Al2O3+2OH-=2AlO2-+H2O.