如图表示某典型金属单质A与其化合物之间的转化关系(某些产物和反应条件已略去).已知:图中所示物质中的组成元素均为短周期元素,化合物C中含有两种金属元素,反应⑤用于工业制取A,反应⑥的产物过滤后得到化合物D的溶液呈碱性.
(1)一步实现图中①至⑥的转化关系中一定属于复分解反应的是______ (填序号).
(2)写出一步实现反应④所需加入的化学试剂(填化学式);______.
(3)写出反应①的离子反应方程式:______.
(4)B→C的转化有多种途径,试写出其中两种不同反应类型的化学反应方程式:______;.______.
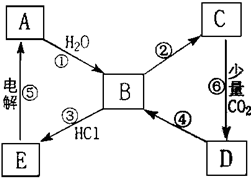
典型金属单质A可与水反应,应为Na,则B为NaCl,E为NaCl,C为NaAlO2,D为Na2CO3,Na2CO3可与Ca(OH)2 或 Ba(OH)2反应生成NaOH,则
(1)由以上物质的转化可知,①Na→NaOH,②NaOH→NaAlO2,③NaOH→NaCl,④Na2CO3→NaOH,⑤NaCl→Na,⑥NaAlO2→Na2CO3,属于复分解反应有③④⑥,
故答案为:③④⑥;
(2)反应④为Na2CO3→NaOH,Na2CO3可与Ca(OH)2 或 Ba(OH)2反应生成NaOH,
故答案为:Ca(OH)2 或 Ba(OH)2;
(3)反应①为Na和水的反应,反应的离子方程式为2Na+2H2O=2Na++2OH-+H2↑,
故答案为:2Na+2H2O=2Na++2OH-+H2↑;
(4)B→C的转化为NaOH→NaAlO2,可通过等Al→NaAlO2,AlCl3→NaAlO2,Al(OH)3→NaAlO2,Al2O3→NaAlO2等反应实现,反应的可分成两种类型:氧化还原:2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
非氧化还原:AlCl3+4NaOH=NaAlO2+3NaCl+2H2O 或Al(OH)3+NaOH=NaAlO2+2H2O或Al2O3+2NaOH=2NaAlO2+H2O.
故答案为:氧化还原:2Al+2NaOH+2H2O=2NaAlO2+3H2↑;非氧化还原:AlCl3+4NaOH=NaAlO2+3NaCl+2H2O 或Al(OH)3+NaOH=NaAlO2+2H2O或Al2O3+2NaOH=2NaAlO2+H2O.

