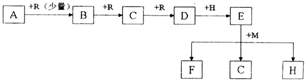
在常温、常压下R为气体单质,B、M为固体单质,A、C、D、E、F、H为化合物,A、C为气体,它们之间的相互转换关系如下图所示(反应所需条件未注明,某些反应已将水等次要产物略去)
请回答下列问题:
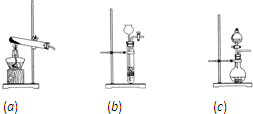
(1)实验室快速制取少量R的方程式为______,发生装置可以选取下列装置中的______(填字母)
(2)若F溶于水得到蓝色溶液,则M为______,E与M反应的化学方程式为______,取50ml物质的量浓度为18mol•L-1的E溶液与足量的M在加热条件下充分反应,得到气体C在标准状况下的体积为V L,下列说法中正确的是:______
(A)V<10.08
(B)因为M为足量,可以计算出被还原的E的物质的量为0.45mol
(C)被氧化的M的质量为
g20V 7
(D)若将生成的气体C通入紫色石蕊试液中,溶液先变红,最终褪为无色.
(E)可以用BaCl2溶液来检验最终溶液中E有无剩余.
(3)若M为短周期元素形成的黑色固体单质,实验室利用下图装置检验E和M在加热条件下反应所得全部产物.
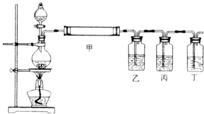
①装置甲中应加的试剂是______;
②装置乙、丙和丁中所加试剂分别是______(填下列选项的字母序号)
(A)澄清石灰水、品红溶液、高锰酸钾酸性溶液
(B)品红溶液、高锰酸钾酸性溶液、澄清石灰水
(C)澄清石灰水、高锰酸钾酸性溶液、品红溶液
③在实验中如果将丙去掉,______(填“能”或“不能”)达到实验目的,原因是______.
④如果将烧瓶中产生的气体混合物分别通入Ba(NO3)2溶液和BaCl2溶液中,二者现象______(填“会”或“不会”).
相同(4)若M为短周期元素形成的单质,用它制作的容器在常温下能够盛放E的浓溶液.请写出M的单质与E的浓溶液剧烈反应的化学方程式______.
(1)气体化合物A与少量气体单质R反应,生成固体单质B,B与R反应生成C,C与R反应生成D,所以A为H2S,B为S,C为SO2、D为SO3,实验室中快速制取氧气用二氧化锰催化分解过氧化氢的方法,该方法不需加热,由于固体是粉末,所以不能用装置b.故答案为:2H2O2
2H2O+O2↑;C; MnO2 .
(2)若F溶于水得到蓝色溶液,则F中含有铜离子,M为铜,M与E反应生成三种物质,其中有C,推出E为硫酸、H为水、F为硫酸铜,故E与M反应的化学方程式为:Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O;若浓硫酸完全反应,生成10.08L二氧化硫,但随反应进行,硫酸浓度变小,反应停止,所以生成的气体小于10.08L,A对B错;根据反应方程式知,生成气体的物质的量与M被氧化的物质的量相等,C对;二氧化硫只能使紫色石蕊溶液变红,D错;反应生成物业能与氯化钡反应生成沉淀,D错;故正确的为A、C; △ .
故答案为:Cu;Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O;A、C; △ .
(3)①若M为短周期元素形成的黑色固体单质,则M为碳.与浓硫酸反应生成水、二氧化碳和二氧化硫.检验三种产物时应先检验水,所以甲中物质为无水硫酸铜,用于检验水,
故答案为:无水硫酸铜;
②乙中盛放品红溶液,检验二氧化硫,用丁中的澄清石灰水检验二氧化碳,但要先除去二氧化硫,因为二氧化硫也能使石灰水变浑浊,所以丙的作用是除去二氧化硫,可用溴水或高锰酸钾溶液.故答案为:B;
③在实验中如果将丙去掉,SO2也能使澄清石灰水变浑浊,必须先除尽SO2后再检验CO2,以防SO2的干扰,故答案为:不能;SO2也能使澄清石灰水变浑浊,必须先除尽SO2后再检验CO2,以防SO2的干扰;
④烧瓶中产生的气体混合物含有二氧化硫和二氧化碳,通入硝酸钡溶液,有硝酸生成,将亚硫酸钡氧化为硫酸钡沉淀,通入氯化钡溶液则没有沉淀生成,故答案为:不会;
(4)M为短周期元素形成的单质,用它制作的容器在常温下能够盛放浓硫酸,则M为铝,与浓硫酸反应生成硫酸铝、二氧化硫和水,
故答案为:2Al+6H2SO4(浓)
Al2(SO4)3+3SO2↑+6H2O. △ .