如图是A~O 的转化关系.已知A是一种金属单质,B、C、D、E、F、H、I、J、K常温常压下均为气体,且B、C、D、E是单质,I是一种红棕色气体,G是一种淡黄色固体,M是混合物,含有气体,J与K相遇会产生大量白烟.请回答下列问题:
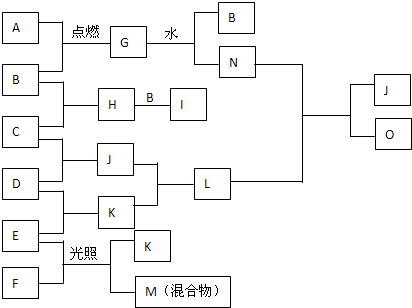
(1)写出G与水反应的化学方程式______;写出气体E与N溶液反应的离子方程式______.
(2)化合物G中含有的化学键为______.
(3)写出F的电子式______,化合物O的电子式______.
(4)E与F反应生成气体的化学方程式为______.
G是一种淡黄色固体,结合转化G+H2O→B+N,故G为Na2O2,B是气体单质,故B为O2,N为NaOH,A是一种金属单质,结合A+B→G可知,A为Na;
I是一种红棕色气体,为NO2,B为O2,由H
I可知H为NO,C为气体单质,由B+C→H可知,C为N2;B
J、K为气体,J与K相遇会产生大量白烟,为HCl与NH3,故L为NH4Cl,C为N2,D气体单质,由转化关系C+D→J,故J为NH3,
K为HCl,D为H2,由转化D+E→K,且E为气体单质,故E为Cl2,由转化E+F
K+M(混合物),M含有气体,且F为气体,考虑甲烷与氯气反应符合转化关系,故F为CH4,M为甲烷的卤代物;光照
N为NaOH,L为NH4Cl,由N+L→J+O,且J为NH3,O为NaCl;
(1)G为Na2O2,与水反应生成氢氧化钠与氢气,反应方程式为:2Na2O2+2H2O=4NaOH+O2↑;
E为Cl2,N为NaOH,氯气与氢氧化钠反应反应生成氯化钠、次氯酸钠、水,反应离子方程式为:Cl2+2OH-=Cl-+ClO-+H2O,
故答案为:2Na2O2+2H2O=4NaOH+O2↑;Cl2+2OH-=Cl-+ClO-+H2O;
(2)Na2O2是离子化合物,钠离子与过氧根离子之间形成离子键,过氧根离子中氧原子之间形成共价键,故答案为:离子键、共价键;
(3)F为CH4,分子中碳原子与氢原子之间形成1对共用电子对,电子式为:
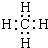
;
O为NaCl,是离子化合物,由钠离子与氯离子构成,电子式为:
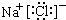
,故答案为:
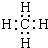
;
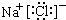
;
(4)氯代甲烷中一氯甲烷是气,E与F反应生成气体的反应是甲烷与氯气反应生成一氯甲烷与氯化氢,反应反应方程式为CH4+Cl2
CH3Cl+HCl,光照
故答案为:CH4+Cl2
CH3Cl+HCl.光照
