(09泰州) (11分)钢铁、铝合金、铜制品等是应用广泛的金属材料。据估计,每年全世界被腐蚀损耗的钢铁材料,约占全年钢产量的十分之一。某校化学兴趣小组的同学探究金属腐蚀的原因,设计如下实验:
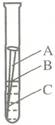
(1)如图,取一根约10cm的光亮铁钉放在自来水中,观察A、B、C三处的变化。几天后,他们会发现 ▲ 处最先出现铁锈,大家结合书本知识知道,铁在空气中生锈实际是铁和 ▲ 、 ▲ 等物质相互作用发生一系列复杂的化学反应的过程。
(2)一同学联想到家里铜制餐具上有一层绿色物质,认为铜在空气中也会生锈。他们上网查阅资料,知道这种绿色物质的化学成分为Cu2(OH)2CO3(铜绿)。他们从铜绿组成和空气的成分大胆猜测,铜生锈除了与铁生锈条件相同外,还应该有CO2参加反应。
请写出铜在空气中生成铜绿的化学方程式 ▲ 。
(3)【查阅资料】孔雀石的主要成分是Cu2(OH)2CO3,也可以表示成CuCO3·Cu(OH)2。与孔雀石相似,还有许多矿物可用xCuCO3·yCu(OH)2(x、y都是正整数)表示,石青就是其中的一种。
【实验探究】为了验证石青的组成成分,他们设计了如下实验,请你共同参与探究。
| 实验操作 | 实验现象 | 结论 | |
| 步骤l | 取少量石青样品置于大试管中加入足量稀硫酸 | (1)产生大量气体 (2)溶液呈蓝色 | (1)石青中含有 ▲ 离子 (2)石青中含有 ▲ 离子 |
| 步骤2 | 取少量石青样品置于大试管中加热 | (1)残留固体呈 ▲ 色 (2)大试管内壁 ▲ | 石青加热易分解 |
【反思与拓展】
①确定步骤1中产生气体成分的实验方法是 ▲ 。
②根据以上探究,只要测定出参加反应的石青的质量、生成的氧化铜的质量和 ▲ 的质量,就可确定石青的化学式(即确定x、y的值)。
③防止金属锈蚀的方法很多,如制成不锈钢、在金属表面 ▲ (任写一种方法)。
(1) B O2或氧气 H2O或水 (2) 2Cu+O2+H2O+CO2 ===Cu2(OH)2CO3
(3) 【查阅资料】CO32- Cu2+ 黑 有水珠
【反思与拓展】
①将产生的气体通入足量的澄清石灰水中 ②水或二氧化碳 ③涂油、漆等
分析:钢铁生锈的条件是钢铁与氧气和水同时接触.防止金属生锈的方法有:在金属表面涂一层油漆;在金属表面镀一层金属等.
根据反应物和生成物及其质量守恒定律可以书写化学方程式.
根据实验现象可以确定物质的组成.
二氧化碳能使澄清的石灰水变浑浊.
解答:解:(1)B处与水和氧气充分接触,容易生锈.故填:B.
(2)铜在空气中生成铜绿的化学方程式为:2Cu+O2+H2O+CO2═Cu2(OH)2CO3.
(4)样品和稀硫酸反应能生成大量气体,说明样品中含有碳酸根离子,溶液呈蓝色说明样品中含有铜离子.
样品在大试管中加热能生成氧化铜和水,氧化铜是黑色的,大试管内壁应该有水珠出现.
| 实验操作 | 实验现象 | 结论 | |
| 步骤1 | (1)碳酸根 (2)铜 | ||
| 步骤2 | (1)黑 (2)出现水珠 |
②根据以上探究,只要测定出参加反应的石青的质量、生成的氧化铜的质量和水与二氧化碳的质量,就可确定石青的化学式(即确定x、y的值).故填:水与二氧化碳.
③防止金属锈蚀的方法很多,如制成不锈钢、在金属表面涂油、漆等.故填:涂油、漆等.
