某化学兴趣小组用含A、B两种金属单质的粉末状混合物进行如下实验,其转化关系如图所示(部分反应物和生成物未列出),其中E为白色沉淀,I为红褐色沉淀.
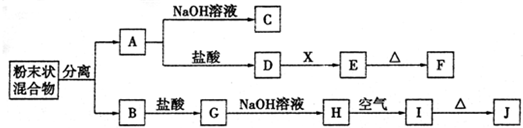
(此转化关系中所用的试剂都是足量的)
(1)写出下列物质的化学式:F______,G______.
(2)将混合物中两种金属分离开的最简单的方法是______.
(3)D→E的转化中,加入过量的X可能是______.
(4)写出下列转化的方程式:
A→C(离子方程式):______;H→I(化学方程式):______;G→H(离子方程式):______.
I为红褐色沉淀,为Fe(OH)3,由转化关系可知,H为Fe(OH)2,G为FeCl2,B为Fe;
金属A能与盐酸、氢氧化钠溶液反应,A为金属Al,E为白色沉淀,为Al(OH)3,由转化关系可知,D为AlCl3,X为碱或水解为碱性的物质,F为Al2O3,
(1)由上述分析可知,F为Al2O3,G为FeCl2;
故答案为:Al2O3,FeCl2;
(2)混合物为铁与铝,铁具有磁性,可以利用磁铁吸出铁进行分离;
故答案为:利用磁铁吸出铁;
(3)D→E的转化为AlCl3→Al(OH)3,X为碱或水解为碱性的物质,加入过量的X,X不能是强碱,故X可能是氨水(或碳酸钠、碳酸氢钠、偏铝酸钠)等;
故答案为:氨水(或碳酸钠、碳酸氢钠、偏铝酸钠等);
(4)A→C为铝与氢氧化钠溶液反应生成偏铝酸钠与氢气,离子方程式为:2Al+2OH-+2H2O=2AlO2-+3H2↑;
H→I为氢氧化亚铁被氧化为氢氧化铁,反应方程式为:4Fe(OH)2+O2+2H2O=4Fe(OH)3;
G→H为氯化亚铁与氢氧化钠反应生成氢氧化亚铁、氯化钠,反应离子方程式为:Fe2++2OH-=Fe(OH)2↓;
故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;4Fe(OH)2+O2+2H2O=4Fe(OH)3;Fe2++2OH-=Fe(OH)2↓;
