A、B、C为三种常见的单质,其中A、C为气体,B为常见金属.A溶于水所得的溶液可使石蕊试液先变红后退色.F的水溶液为浅绿色溶液,它们的关系如图:
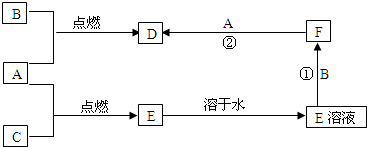
(1)写出A、B、D的化学式:
A.______ B.______ D.______
(2)写出反应①②的离子方程式
①______
②______
(3)检验D的水溶液中的阳离子的方法是:______.将D溶液逐滴加入的沸水中会产生一种红褐色的澄清液体.有同学认为该液体中的分散质粒子直径应该在1nm~100nm之间,验证这一想法的简单方法是:______
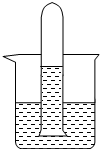
(4)如图某同学将A的饱和溶液装满大试管倒置于烧杯中,光照一段时间后,发现试管底部有无色的气体产生,溶液的颜色也变成无色,请你帮他对产生的气体进行探究:
a.你预测气体可能是______、______
b.针对你的预测写出验证实验方案:______.
(1)A溶于水所得的溶液可使石蕊试液先变红后退色,则说明A为Cl2,与水反应生成HCl和HClO,能使石蕊试液先变红后褪色,F的水溶液为浅绿色溶液,说明B中含有Fe2+,能继续和Cl2反应生成D,则D为FeCl3,所以B为Fe,则C为H2,E为HCl,故答案为:Cl2;Fe;FeCl3;
(2)①反应①为Fe和盐酸的反应,反应的离子方程式为Fe+2H+═Fe2++H2↑,故答案为:Fe+2H+═Fe2++H2↑;
②FeCl2具有还原性,能与具有氧化性的Cl2反应生成FeCl3,反应的离子方程式为2Fe2++Cl2═2Fe3++2Cl-,
故答案为:2Fe2++Cl2═2Fe3++2Cl-;
(3)检验Fe3+,可用KSCN溶液,观察溶液是否变红,具体做法为取少量溶液于试管中,滴加两滴KSCN溶液,观察溶液是否变红色,将饱和FeCl3溶液滴加到沸水中生成氢氧化铁胶体,具有丁达尔效应,
故答案为:取少量溶液于试管中,滴加两滴KSCN溶液,观察溶液是否变红色;是否有丁达尔现象;
(4)a.无色气体可能为氧气或氢气,但Cl2与水反应生成HCl和HClO,根据HClO的不稳定性,易分解生成氧气,故答案为:O2;或H2;
b.根据氢气和氧气的性质碱性检验,氢气易燃烧,氧气能使木条复燃,具体做法是在水下堵住试管口,取出正放,用燃着的木条放在试管口,如果气体燃烧说明是H2;如果木条燃烧更旺说明是O2,
故答案为:在水下堵住试管口,取出正放,用燃着的木条放在试管口,如果气体燃烧说明是H2;如果木条燃烧更旺说明是O2.
