问题
填空题
在下列各变化中,反应①为常温下的反应,A、C、D均含氯元素,且A中氯元素的化合价介于C与D之间,E常温下为无色无味的液体,F为淡黄色粉末,G为常见的无色气体.
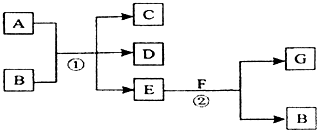
回答下列问题:
(1)A、G的化学式分别为______、______.
(2)A和E反应的离子方程式为_______.
(3)写出反应①的化学方程式______.
(4)在反应②中,每生成2.24L气体G(标准状况)时,消耗F______g.
答案
E常温下为无色无味的液体,应为H2O,F为淡黄色粉末,应为Na2O2,则G为O2,B为NaOH,A、C、D均含氯元素,且A中氯元素的化合价介于C与D之间,应为Cl2和NaOH的反应,生成NaCl和NaClO,
(1)由以上分析可知A为Cl2,G为O2,故答案为:Cl2; O2;
(2)A为Cl2,E为H2O,二者反应的离子方程式为Cl2+H2O=H++Cl-+HClO,
故答案为:Cl2+H2O=H++Cl-+HClO;
(3)反应①为Cl2和NaOH的反应,生成NaCl和NaClO,反应的离子方程式为Cl2+2NaOH=NaCl+NaClO+H2O,
故答案为:Cl2+2NaOH=NaCl+NaClO+H2O;
(4)n(O2)=
=0.1mol,反应的方程式为2Na2O2+2H2O=4NaOH+O2↑,根据方程式可知消耗n(Na2O2)=0.2mol,2.24L 22.4L/mol
则m(Na2O2)=0.2mol×78g/mol=15.6g,
故答案为:15.6.
