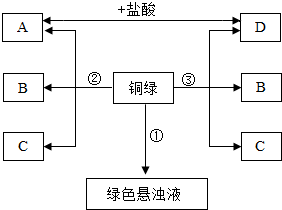
小彤的一副眼镜戴了一段时间后,发现铜质镜架上出现了一墨绿色物质,他想将其除掉.经查阅资料得知:铜在一定条件下会锈蚀生成一种绿色物质,其主要成分是碱式碳酸铜(俗称铜绿),于是他和几个同学按如下方案进行了实验.
试填空
(1)实验①是向铜绿中加入适量常见无色液体B,再加热至沸,沉淀仍然不变色.实验②、③中C是一种常见的无色气体,B的化学式为______.为满足实验③反应所需的外界条件,应该使用关键仪器名称是______.
(2)写出实验②反应的化学方程式______,
在此过程中,判断铜绿没有完全反应的现象是______.
(3)将A的溶液5~9滴滴入5mL10%的氢氧化钠溶液中得到蓝色絮状沉淀,稍加热即变黑色沉淀D.写出蓝色絮状沉淀转变为D的化学方程式______.
(4)已知Ca(HCO3)2
CaCO3↓+H2O+CO2↑,则热稳定性CaCO3>Ca(HCO3),由此推理上述实验中铜绿、蓝色絮状沉淀、物质D三种化合物热稳定性由强至弱的顺序是:______>______>______(均写化学式). △ .
(5)经过讨论.同学们建议小彤可以用______除去镜架上的绿色物质..
(1)碱式碳酸铜受热分解能生成氧化铜、水和二氧化碳,和盐酸反应能生成氯化铜、水和二氧化碳;氧化铜和盐酸反应能生成氯化铜和水;所以C是二氧化碳,B是水.故填:H2O;酒精灯.
(2)碱式碳酸铜和盐酸反应的化学方程式为:Cu2(OH)2CO3+4 HCl═2CuCl2+3H2O+CO2↑.
在此过程中,判断铜绿没有完全反应的现象是绿色沉淀没有全部溶解.故填:绿色沉淀没有全部溶解.
(3)蓝色絮状沉淀是氢氧化铜,氢氧化铜受热分解能生成氧化铜和水,反应的化学方程式为:Cu(OH)2
CuO+H2O. △ .
(4)由于加热氢氧化铜和碱式碳酸铜都能生成氧化铜,所以氧化铜的热稳定性强,
氢氧化铜不稳定,空气中就会失水发黑,90℃左右即开始分解为CuO;碱式碳酸铜分解温度高于100℃,空气中可以稳定存在.所以碱式碳酸铜的热稳定性比氢氧化铜的热稳定性强.
故填:CuO;Cu2(OH)2CO3;Cu(OH)2.
(5)可以用盐酸除去镜架上的绿色物质.故填:盐酸.
