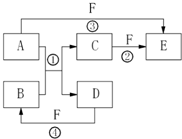
A、B、C、D、E、F六种物质的相互转化关系如右图所示(反应条件及部分产物未列出).
(1)若A是常见金属单质,与B的水溶液反应生成C和D.D、F是气体单质,D在F中燃烧时发出苍白色火焰.则反应②(在水溶液中进行)的离子方程式为______.
(2)若A、D为短周期元素组成的固体单质,一种为金属,另一种为非金属.且③④两个反应都有红棕色气体生成,则反应④的化学方程式为______.
(3)若A是黑色固体,D是有臭鸡蛋气味的气体,E溶液中滴加KSCN溶液呈血红色.则D的电子式是______;工业上生产B的第一个生产阶段是煅烧与A含相同元素的矿石,其化学方程式是______,使用的设备是______.
(4)若B是由地壳中含量最高的两种元素组成,A的一种同素异形体与B、D属同一种类型的晶体,则反应①的化学方程式是______,B与烧碱溶液反应的化学方程式是______.
(1)D、F是气体单质,D在F中燃烧时发出苍白色火焰,应是在中的燃烧反应,则D、F应分别为H2、Cl2,B为HCl,A应为Fe,C为FeCl2,E为FeCl3,反应②为FeCl2被氧化生成FeCl3的反应,离子方程式为2Fe2++Cl2=2Fe3++2Cl-,
故答案为:2Fe2++Cl2=2Fe3++2Cl-;
(2)A+B=C+D是置换反应,若A、D为短周期元素单质,且A为固体金属单质,D为固体非金属单质,③和④两个反应中都有红棕色气体生成,非金属单质D为C,F为浓硝酸,金属置换非金属单质的反应应为镁和二氧化碳反应生成氧化镁和碳的反应,判断A为Mg;B为CO2;C为MgO;D为C;E为Mg(NO3)2;F为NHO3,
浓HNO3与C反应的化学方程式为C+4HNO3(浓)
CO2↑+4NO2↑+2H2O, △ .
故答案为:C+4HNO3(浓)
CO2↑+4NO2↑+2H2O; △ .
(3)若A是黑色固体,D是有臭鸡蛋气味的气体,应为H2S,电子式为
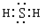
,E溶液中滴加KSCN溶液呈血红色,说明E溶液中含有Fe3+,A应为FeS2,F应为氧化性酸,可为HNO3,则B为H2SO4,FeS2与O2的反应为工业制备硫酸的重要反应,在沸腾炉中进行,反应的方程式为4FeS2+11O2
2Fe2O3+8SO2, △ .
故答案为:
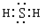
; 4FeS2+11O2
2Fe2O3+8SO2;沸腾炉; △ .
(4)B是由地壳中含量最高的两种元素组成,应为SiO2,为原子晶体,则A应为C,D为Si,C为CO,F为O2,E为CO2,
反应①的化学方程式是2C+SiO2
Si+2CO↑,SiO2可与烧碱反应,方程式为SiO2+2NaOH=Na2SiO3+H2O, △ .
故答案为:2C+SiO2
Si+2CO↑; SiO2+2NaOH=Na2SiO3+H2O. △ .
