图中A~X分别代表一种反应物或生成物,其中F、G、X为单质,短周期元素X原予的核电荷数是其最外层和最内层电子数之和的3倍.已知A受热分解得到等物质的量的B、C、D三种气态物质,D气体能使湿润的红色石蕊试纸变蓝色,其它为化合物,图中部分生成物未列出.

请回答:
(1)B的电子式______,写出F的一种同素异形体______,D分子的空间构型为______.
(2)写出反应B与X反应的化学方程式______.
(3)写出A与足量K溶液加热时反应的离子方程式______.
(4)在一定条件下,2L的H气体与0.5L的G气体相混合,若该混合气体被NaOH溶液恰好完全吸收,只生成一种盐.请写出该反应过程中总的化学反应方程式:______.
(5)在F与J的反应中当转移了1.5mol电子时,产生标准状况下的I气体的体积为______L.
短周期元素X原予的核电荷数是其最外层和最内层电子数之和的3倍,应为Mg元素,A受热分解得到等物质的量的B、C、D三种气态物质,应为NH4HCO3,分解可生成NH3、CO2和H2O,D气体能使湿润的红色石蕊试纸变蓝色,应为NH3,能在B中燃烧的应为CO2和Mg的反应,则C为H2O,B为CO2,K为NaOH,G为O2,H为NO,I为NO2,F为单质,应为C,则E为MgO,
J为HNO3,则
(1)由以上分析可知B为CO2,电子式为
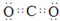
,F为C,对应的同素异形体有金刚石、C60、石墨等,D为NH3,为三角锥形结构,
故答案为:
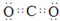
;金刚石(C60、石墨等);三角锥形;
(2)CO2和Mg反应生成MgO和C,反应的方程式为2Mg+CO2
2MgO+C, 点燃 .
故答案为:2Mg+CO2
2MgO+C; 点燃 .
(3)NH4HCO3与足量KOH溶液加热时反应的离子方程式为NH4++HCO3-+2OH-
NH3↑+CO32-+2H2O, △ .
故答案为:NH4++HCO3-+2OH-
NH3↑+CO32-+2H2O; △ .
(4)2L的NO气体与0.5L的O2气体相混合,若该混合气体被NaOH溶液恰好完全吸收,反应的方程式为4NO+O2+4NaOH=4NaNO2+2H2O,
故答案为:4NO+O2+4NaOH=4NaNO2+2H2O;
(5)C和HNO3反应被氧化为CO2,同时硝酸被还原为NO2,N元素化合价降低1价,则反应中当转移了1.5mol电子时,生成1.5molNO2,体积为33.6L,
故答案为:33.6.
