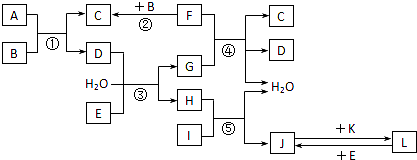
下列转化关系图中,A、B、C、D、E常温下为气体,B、E、F、K为单质,其中F为黑色固体;C、D均能使澄清石灰水变浑浊,D、E均能使品红溶液褪色;I是一种红棕色固体氧化物.请回答下列问题:
(1)C的电子式为______;
(2)检验溶液L中金属阳离子的方是______;
(3)反应③的离子方程式为______;
(4)F和G的浓溶液反应的化学方程式为______;
(5)气体A的密度为2.68g/L(标准状况),通过计算、推理,可确定A的分子式为______.
A、B、C、D、E常温下为气体,C、D均能使澄清石灰水变浑浊,D、E均能使品红溶液褪色,则D为SO2,C为CO2,B、E、F、K为单质,则反应①为含S、C与氧气的反应;E为Cl2,反应③为氯气、二氧化硫反应生成硫酸和盐酸,反应④为C与浓硫酸的反应,反应②为C与氧气反应生成二氧化碳,则G为H2SO4,H为HCl,I是一种红棕色固体氧化物,I为Fe2O3,反应⑤为盐酸与氧化铁的反应,J为FeCl3,K为Fe,L为FeCl2,
(1)C为CO2,其电子式为

,故答案为:

;
(2)L中含有的阳离子为亚铁离子,则向溶液中滴加KSCN溶液无现象,滴加氯水,溶液变为红色(或向溶液中加入碱,产生的沉淀迅速变为灰绿色,最终变为红褐色),
故答案为:向溶液中滴加KSCN溶液无现象,滴加氯水,溶液变为红色(或向溶液中加入碱,产生的沉淀迅速变为灰绿色,最终变为红褐色);
(3)反应③的离子方程式为Cl2+2H2O+SO2=4H++2Cl-+SO42-,故答案为:Cl2+2H2O+SO2=4H++2Cl-+SO42-;
(4)F和G的浓溶液反应的为C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O,故答案为:C+2H2SO4(浓) △ .
CO2↑+2SO2↑+2H2O; △ .
(5)气体A的密度为2.68g/L(标准状况),其摩尔质量为22.4L/mol×2.68g/L=60g/mol,A中含有S、C元素,60-32-12=16,则还含有O,即A为SCO,故答案为:SCO.