A、B、C、D、E为中学化学常见物质,其中A、C为金属单质,E为非金属单质,下图是它们之间的相互转化关系.请回答:
(1)反应①的基本反应类型是______;
(2)C的化学式为______;
(3)写出物质E和B在加热条件下反应的化学方 程式______;
(4)将浅绿色溶液D转化为黄色溶液的方法是(用离子方程式表示)______.
(5)乙醇在A作催化剂的条件下可以被空气中的氧气催化氧化,试写出该反应的化学方程式:______.
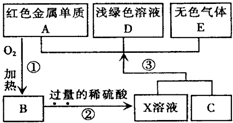
由A为红色金属单质,则A为Cu,由反应①可知B为CuO,由反应②X为硫酸铜、硫酸混合溶液,由反应③X溶液+C→A+D+E,且D为浅绿色溶液(含有Fe2+),E为无色气体,故C为Fe,D为FeSO4,E为H2,
(1)反应①是2Cu+O2
2CuO,属于化合反应,故答案为:化合反应; 点燃 .
(2)由上述分析可知,C为Fe,故答案为:Fe;
(3)H2和CuO在加热条件下反应是Cu与H2O,反应方程式为:H2+CuO
Cu+H2O,故答案为:H2+CuO △ .
Cu+H2O; △ .
(4)利用强氧化剂将浅绿色FeSO4溶液转化为黄色Fe2(SO4)3溶液,如加入氯水等,反应离子方程式为:2Fe2++Cl2=2Fe3++2Cl-,
故答案为:2Fe2++Cl2=2Fe3++2Cl-;
(5)乙醇在Cu作催化剂的条件下可以被空气中的氧气催化氧化生成乙醛与水,该反应的化学方程式为:2CH3CH2OH+O2
2CH3CHO+2H2O,Cu
故答案为:2CH3CH2OH+O2
2CH3CHO+2H2O.Cu
