已知D、M、H是常见的非金属单质,其中M是无色气体,H是有色气体,J是一种金属单质(其同族的某种元素是形成化合物种类最多的元素),A、C是金属氧化物,C和J均是某种常见电池的电极材料,J元素的+2价化合物比+4价化合物稳定,B与C反应时,每生成1molH同时消耗4molB和1molC,K只知含有CO 或CO2中的一种或两种.它们关系如图:
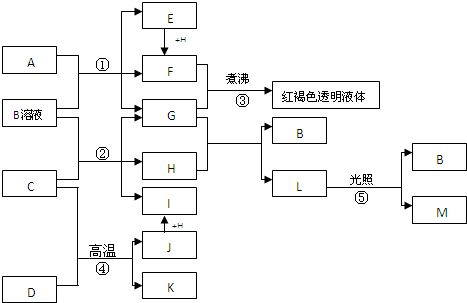
(1)写出下列物质的化学式:A______ D______
(2)写出下列反应的化学方程式:
②______
⑤______
(3)由金属氧化物A和C得到其相应的金属,在冶金工业上一般可用______方法(填序号)
①热分解法 ②热还原法 ③电解法
其中从A得到其相应金属也可用铝热法,若反应中1molA参加反应,转移电子的物质的量为______
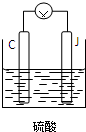
(4)用C、J作电极,与硫酸构成如图所示电池,正极的电极反应为______当反应转移1mol电子时,负极质量增加______g.
H是有色气体判断为Cl2,J是一种金属单质(其同族的某种元素是形成化合物种类最多的元素)推断为Pb,J+H=I,可以判断I为PbCl2,A、C是金属氧化物,C和J均是某种常见电池的电极材料,J元素的+2价化合物比+4价化合物稳定,C为PbO2,K只知含有CO 或CO2中的一种或两种,结合C+D=J+K 可知此反应为是碳和PbO2的反应,判断为D为C;F+G=红褐色液体证明生成的是氢氧化铁胶体,E+H=F,A+B=E+F+G 推断E为FeCl2;F为FeCl3;G为H2O;B为HCl;A为Fe3O4;依据G+H=B+L可知L为HClO,M为O2;B与C反应时,每生成1molH同时消耗4molB和1molC,判断反应PbO2+4HCl=2H2O+Cl2↑+PbCl2;推断出的物质为:A、Fe3O4 ;B、HCl;C、PbO2 ;D、C;E、FeCl2;F、FeCl3;G、H2O;H、Cl2;L、HClO;J、Pb;K、CO、CO2;I、PbCl2;M、O2;
(1)A物质的化学式为:Fe3O4;D的化学式为C,故答案为:Fe3O4;C;
(2)②是B与C反应时,每生成1molH同时消耗4molB和1molC,化学方程式为:PbO2+4HCl(浓)═PbCl2+Cl2↑+2H2O;⑤是次氯酸见光分解的反应,化学方程式为:2HClO═2HCl+O2↑,
故答案为:PbO2+4HCl(浓)═PbCl2+Cl2↑+2H2O;2HClO═2HCl+O2↑;
(3)由金属氧化物A为Fe3O4和C为PbO2 得到其相应的金属为Fe、Pb,依据金属活动顺序表中 金属冶炼的方法分析判断,在冶金工业上一般可用热还原法:故选②; 其中从A得到其相应金属也可用铝热法,发生的反应为3Fe3O4+8Al
9Fe+4Al2O3;若反应中1molA参加反应,转移电子的物质的量为8mol, 高温 .
故答案为:②;8mol;
(4)用C、J作电极,与硫酸构成如图所示电池是铅蓄电池,正极为PbO2;电极反应为:PbO2+2e-+4H++SO42-═PbSO4+2H2O;负极为Pb;电极反应为:Pb+SO42--2e-=PbSO4; 当反应转移1mol电子时,反应0.5molPb质量=0.5mol×207.2g/mol=103.6g,生成0.5molPbSO4质量=0.5mol×303.2g/mol=151.6g;负极质量增加=151.6g-103.6g=48g,
故答案为:PbO2+2e-+4H++SO42-═PbSO4+2H2O;48.
