已知A~N分别代表一种物质,它们之间的转化关系如图所示(部分反应的反应条件和生成物已略去).A、B、C分别是由短周期元素组成的单质,A是金属,D是无色液体.F是一种离子化含物,其阴阳离子的个数比为1:3,且能与水反应得到两种碱.反应①是实验室检验某离子的方法,反应②是工业、生产N的重要反应.请回答下列问题:
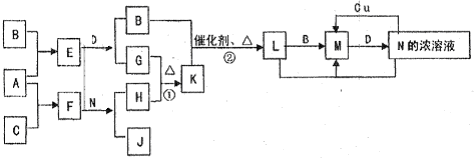
(1)B元素在元素周期表中的位置是______,F的电子式是______.
(2)写出反应①的离子方程式:______
(3)Cu与足量的N的浓溶液反应得到的产物主要是M不是L,其原因是______
(请用上图所示关系中反应的化学方程式回答).
(4)选择性催化还原(SCR)是在有催化剂的条件下将M转变为无毒的物质,这是目前国外进行尾气治理遍采用的一种方法.亚铬酸铜(Adkin偿化剂)是极好的M催化还原的催化剂,是铜和铬的复合氧化物,成分不固定,如:aCuO•bCr2O3等,统称为亚铬酸铜.
CuNH4(OH)CrO4在295℃分解生成复合的氧化物(催化剂)、氮气及水,写出该反应的化学方程式:______.
(5)已知一定温度(>100℃)下,反应②的平衡常数为1.将0.8mol K和1.1mol B放入容积为1L的封闭容器中,发生反应②,一段时间后L的浓度为0.4mol/L,此时反应v正______v逆(填“>”、“<”或“=”). 当反应到达平衡后,保持温度不变,再加入一定物质的量的B,重新达到平衡,则L的平衡浓度______(填“增大”、“不变”或“减小”),B的转化率______.(填“升高”、“不变”或“降低”),L的体积分数______(填“增大”、“不变”、“减小”或“无法确定”).
A是金属,D是无色液体.F是一种离子化含物,其阴阳离子的个数比为1:3,且能与水反应得到两种碱,则A为Na,D为H2O,由K、L、M的转化可知,K为NH3,L为NO,M为NO2,所以B为氧气,E为过氧化钠,G为NaOH,C为氮气,F为Na3N,H为硝酸铵,
(1)B为O,其原子序数为8,位于元素周期表中第二周期第ⅥA族,F为Na3N,其电子式为
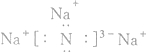
,
故答案为:第二周期第ⅥA族;
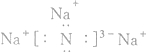
;
(2)反应为铵盐与碱的反应,该反应的离子反应为NH4++OH-
NH3↑+H2O,故答案为:NH4++OH- △ .
NH3↑+H2O; △ .
(3)Cu与足量的N的浓溶液反应得到的产物主要是NO2,NO能被浓硝酸氧化,反应为NO+2HNO3(浓)═3NO2+H2O,故答案为:NO+2HNO3(浓)═3NO2+H2O;
(4)反应物为CuNH4(OH)CrO4,生成物为复合的氧化物(催化剂)、氮气及水,该反应的反应方程式为2CuNH4(OH)CrO4
2CuO.Cr2O3+N2↑+5H2O, △ .
故答案为:2CuNH4(OH)CrO4
2CuO.Cr2O3+N2↑+5H2O; △ .
(5)4NH3+5O2
4NO+6H2O催化剂 △
开始0.8 1.1 0 0
转化0.4 0.5 0.4 0.6
某时刻0.4 0.6 0.4 0.6
Q=
<1=K,则化学反应向正反应方向进行,所以v正>v逆,(0.4)4×(0.6)6 (0.4)4×(0.6)5
当反应到达平衡后,保持温度不变,再加入一定物质的量的B,平衡正向移动,则L的平衡浓度增大,但B的转化率降低,因L增大的量与总体积的变化的关系不确定,则L的体积分数无法确定,
故答案为:>;增大;降低;无法确定.
